Cho các nguyên tố 11 Na, 19 K, 13 Al, 12 Mg. Chiều tăng dần tính kim loại của chúng là
-
A.
Mg < Al < K < Na.
-
B.
Al < Mg < Na < K.
-
C.
K < Na < Mg < Al.
-
D.
Al < Na < Mg < K.
- Từ Z → Cấu hình e → Vị trí trong BTH.
- Từ vị trí so sánh được tính kim loại của các nguyên tố:
+ Trong cùng một chu kì, theo chiều tăng của điện tích hạt nhân thì tính kim loại giảm dần.
+ Trong cùng một nhóm A, theo chiều tăng của điện tích hạt nhân thì tính kim loại tăng dần.
Cấu hình e nguyên tử:
11 Na: 1s 2 2s 2 2p 6 3s 1 .
19 K: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 .
13 Al: 1s 2 2s 2 2p 6 3s 2 3p 1 .
12 Mg: 1s 2 2s 2 2p 6 3s 2 .
Vị trí tương đối của các nguyên tố trong bảng tuần hoàn:
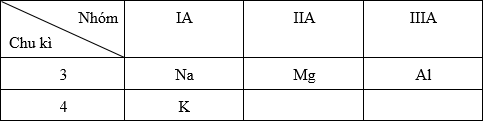
- Trong cùng một chu kì, theo chiều tăng của điện tích hạt nhân thì tính kim loại giảm dần
→ Al < Mg < Na
- Trong cùng một nhóm A, theo chiều tăng của điện tích hạt nhân thì tính kim loại tăng dần
→ Na < K
Vậy tính kim loại: Al < Mg < Na < K.
Đáp án : B