Bài 24. Carboxylic acid trang 86, 87, 88, 89, 90, 91 SBT Hóa 11 Kết nối tri thức
Công thức tổng quát của carboxylic acid no, đơn chức, mạch hở là A. CnH2n+2O2. B. CnH2nO2. C. CnH2n+2O. D. CnH2nO.
24.1
Công thức tổng quát của carboxylic acid no, đơn chức, mạch hở là
A. C n H 2n+2 O 2 . B. C n H 2n O 2 . C. C n H 2n+2 O. D. C n H 2n O.
Phương pháp giải:
Dãy đồng đẳng carboxylic acid đơn chức, no, mạch hở có công thức chung C n H 2n+1 COOH (n ≥ 0) hoặc C n H 2n O 2 (n ≥ 1).
Lời giải chi tiết:
Công thức tổng quát của carboxylic acid no, đơn chức, mạch hở là C n H 2n O 2 .
→ Chọn B .
24.2
Số đồng phân carboxylic acid có công thức phân tử C 4 H 8 O 2 là
A. 2. B. 3. C. 4. D. 5.
Phương pháp giải:
Carboxylic acid là các hợp chất hữu cơ trong phân tử có nhóm carboxyl (−COOH) liên kết với nguyên tử carbon (trong gốc hydrocarbon hoặc – COOH) hoặc nguyên tử hydrogen.
Lời giải chi tiết:
Các đồng phân carboxylic acid có công thức phân tử C 4 H 8 O 2 là
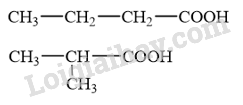
→ Chọn A .
24.3
Khi uống rượu có lẫn methanol, methanol có trong rượu được chuyển hoá ở gan tạo thành formic acid gây ngộ độc cho cơ thể, làm suy giảm thị lực và có thể gây mù. Formic acid có công thức cấu tạo là
A. CH 3 OH. B. HCHO. C. HCOOH. D. CH 3 COOH.
Phương pháp giải:
Formic acid là acid carboxylic có 1 carbon.
Lời giải chi tiết:
Formic acid có công thức cấu tạo là HCOOH.
→ Chọn C .
24.4
Propanoic acid có công thức cấu tạo là
A. CH 3 CH 2 OH. B. CH 3 COOH.
C. CH 3 CH 2 COOH. D. CH 3 CH 2 CH 2 COOH
Phương pháp giải:
Tên theo danh pháp thay thế của carboxylic acid đơn chức:

Lời giải chi tiết:
Propanoic acid có công thức cấu tạo là CH 3 CH 2 COOH.
→ Chọn C .
24.5
(CH 3 ) 2 CHCH 2 COOH có tên gọi theo danh pháp thay thế là
A. dimethylpropanoic acid. B. 2-methylbutanoic acid.
C. 3-methylbutanoic acid. D. pentanoic acid.
Phương pháp giải:
Tên theo danh pháp thay thế của carboxylic acid đơn chức:

Lời giải chi tiết:

24.6
Trong các chất sau đây, chất nào có nhiệt độ sôi cao nhất?
A. CH 3 CH 2 OH. B. CH 3 COOH.
C. CH 3 CHO. D. CH 3 CH 2 CH 2 CH 3 .
Phương pháp giải:
Phân tử carboxylic acid chứa nhóm carboxyl phân cực. Các phân tử carboxyl acid liên kết hydrogen với nhau tạo thành dạng dimer hoặc dạng liên phân tử. Do vậy, carboxylic acid có nhiệt độ sôi cao hơn so với hydrocarbon, alcohol, hợp chất carbonyl có phân tử khối tương đương.
Lời giải chi tiết:
CH 3 COOH có nhiệt độ sôi cao nhất.
→ Chọn B .
24.7
Dung dịch acetic acid không phản ứng được với chất nào sau đây?
A. Mg. B. NaOH. C. Na 2 CO 3 . D. NaCl.
Phương pháp giải:
Carboxylic acid có tính acid yếu:
+ Làm quỳ tím hóa đỏ.
+ Tác dụng với kim loại đứng trước hydrogen trong dãy hoạt động hóa học, giải phóng khí hydrogen.
+ Tác dụng với base, oxide base.
+ Tác dụng với một số muối.
Lời giải chi tiết:
Dung dịch acetic acid là một acid yếu hơn hydrochloric acid (HCl) nên không thể phản ứng được với muối NaCl.
→ Chọn D .
24.8
Khi hoà tan vào nước, acetic acid
A. phân li hoàn toàn. B. phân li một phần.
C. không phân li. D. không tan trong nước.
Phương pháp giải:
Carboxylic acid có tính acid yếu.
Lời giải chi tiết:
Khi hoà tan vào nước, acetic acid phân li một phần. Acetic acid là một acid yếu nên acetic acid là chất điện li yếu.
\({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{CO}}{{\rm{O}}^ - } + {{\rm{H}}^ + }\)
→ Chọn B .
24.9
Nhận định nào sau đây không đúng khỉ nói về tính chất hoá học của acetic acid?
A. Acetic acid là acid yếu, làm đổi màu quỳ tím.
B. Acetic acid có đầy đủ các tính chất của một acid thông thường.
C. Acetic acid phản ứng được với ethanol tạo ester.
D. Acetic acid là acid yếu nên không phản ứng được với đá vôi.
Phương pháp giải:
Tính chất đặc trưng của carboxylic acid là tính acid (làm đổi màu quỳ tím, tác dụng với kim loại, base, oxide base, muối) và phản ứng ester hóa.
Lời giải chi tiết:
Acetic acid có tính acid mạnh hơn carbonic acid. Do đó acetic acid có thể phản ứng với muối của carbonic acid (đá vôi).
2CH 3 COOH + Ca → 2(CH 3 COO) 2 Ca + H 2 ↑
→ Chọn D .
24.10
Một thí nghiệm được mô tả như hình sau đây:

Chất lỏng thu được ở ống nghiệm B có mùi táo, có tên gọi là
A. ethyl formate. B. methyl propionate.
C. ethyl propionate. D. propyl formate.
Phương pháp giải:
Alcohol phản ứng với carboxylic acid tạo ester. Ester sinh ra thường ít tan trong nước, nhẹ hơn nước, nổi lên trên và thường có mùi thơm đặc trưng.
Lời giải chi tiết:
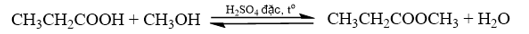
Chất lỏng thu được ở ống nghiệm B có mùi táo, có tên gọi là methyl propionate.
→ Chọn B .
24.11
Acetic acid được điều chế bằng phương pháp lên men giấm từ dung dịch chất nào sau đây?
A. C 2 H 5 OH. B. CH 3 OH. C. CH 3 CHO. D. HCOOH.
Phương pháp giải:
Phương pháp lên men được sử dụng từ thời xa xưa để làm giấm. Nguyên liệu thường dùng là các loại rượu như rượu gạo, rượu táo, rượu vang, … Quá trình lên men nhờ vi khuẩn acetobacter (men giấm) chuyển hoá ethanol thành acetic acid bởi oxygen trong không khí.
Lời giải chi tiết:
Acetic acid được điều chế bằng phương pháp lên men giấm từ dung dịch C 2 H 5 OH.
→ Chọn A .
24.12
Ethyl butanoate là một ester tạo mùi đặc trưng của quả dứa. Viết phương trình hoá học của phản ứng điều chế ethyl butanoate từ acid và alcohol tương ứng.
Phương pháp giải:
Alcohol phản ứng với carboxylic acid tạo ester. Ester sinh ra thường ít tan trong nước, nhẹ hơn nước, nổi lên trên và thường có mùi thơm đặc trưng.
Lời giải chi tiết:
Phương trình hoá học của phản ứng điều chế ethyl butanoate:

24.13
Carboxylic acid X có cấu tạo mạch hở, công thức tổng quát là C n H 2n-2 O 4 . Carboxylic acid X thuộc loại
A. no, đơn chức. B. không no, đơn chức.
C. no và có 2 chức acid. D. không no và có 2 chức acid.
Phương pháp giải:
Công thức tổng quát của carboxylic acid no, đơn chức, mạch hở là C n H 2n O 2 .
Mỗi liên kết π xuất hiện làm mất 2 nguyên tử hydrogen.
Lời giải chi tiết:
Carboxylic acid X có cấu tạo mạch hở, công thức tổng quát là C n H 2n-2 O 4 . Carboxylic acid X thuộc loại no và có 2 chức acid.
→ Chọn C .
24.14
Số đồng phân cấu tạo carboxylic acid và ester có cùng công thức phân tử C 4 H 8 O 2 là
A. 4. B. 3. C. 6. D. 5.
Phương pháp giải:
Carboxylic acid là các hợp chất hữu cơ trong phân tử có nhóm carboxyl (−COOH) liên kết với nguyên tử carbon (trong gốc hydrocarbon hoặc – COOH) hoặc nguyên tử hydrogen.
Ester đơn chức có công thức chung là RCOOR' , trong đó R là gốc hydrocarbon hoặc H ; R' là gốc hydrocarbon.
Lời giải chi tiết:
Các đồng phân cấu tạo carboxylic acid và ester có cùng công thức phân tử C 4 H 8 O 2 là
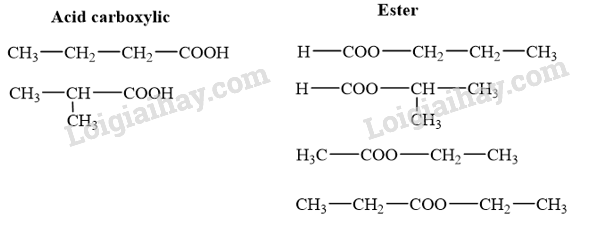
→ Chọn C .
24.15
(CH 3 ) 2 C=CHCOOH có tên gọi theo danh pháp thay thế là
A. 1,1-dimethylpropenoic acid. B. 3,3-dimethylpropenoic acid.
C. 2-methylbut-2-enoic acid. D. 3-methylbut-2-enoic acid.
Phương pháp giải:
Tên theo danh pháp thay thế của carboxylic acid đơn chức:

Lời giải chi tiết:

→ Chọn D .
24.16
Benzoic acid và muối sodium của nó có tác dụng ức chế sự phát triển của nấm mốc, nấm men và một số vi khuẩn khác nên thường được sử dụng làm chất bảo quản thực phẩm. Benzoic acid có công thức cấu tạo là
A. CH 3 COOH. B. HCOOH. C. C 6 H 5 COOH. D. (COOH) 2 .
Phương pháp giải:
Benzoic acid là acid có chứa vòng benzene.
Lời giải chi tiết:
Công thức của benzoic acid là C 6 H 5 COOH.
→ Chọn C .
24.17
Dãy nào sau đây gồm các chất có nhiệt độ sôi tăng dần từ trái qua phải?
A. C 4 H 10 , C 2 H 5 OH, CH 3 CHO, HCOOH, CH 3 COOH.
B. C 2 H 5 OH, C 4 H 10 , CH 3 CHO, CH 3 COOH, HCOOH.
C. CH 3 CHO, C 2 H 5 OH, HCOOH, CH 3 COOH, C 4 H 10 .
D. C 4 H 10 , CH 3 CHO, C 2 H 5 OH, HCOOH, CH 3 COOH.
Phương pháp giải:
- Với các hợp chất có khối lượng phân tử tương đương:
Thứ tự tăng dần về nhiệt độ sôi của các chất là: alkane < aldehyde < alcohol < carboxylic acid.
- Với các hợp chất cùng nhóm chức, nhiệt độ sôi tăng theo chiều tăng của khối lượng phân tử.
Lời giải chi tiết:
Các chất có nhiệt độ sôi tăng dần từ trái qua phải:
C 4 H 10 , CH 3 CHO, C 2 H 5 OH, HCOOH, CH 3 COOH.
→ Chọn D.
24.18
Giấm ăn được dùng phồ biến trong chế biến thực phẩm, có chứa acetic acid với hàm lượng 4-8% về thể tích. Một chai giấm ăn thể tích 500 mL có hàm lượng acetic acid là 5%, thể tích acetic acid có trong chai giấm ăn đó là
A. 5 mL. B. 25 mL. C. 50 mL. D. 100 mL.
Phương pháp giải:
Sử dụng công thức: \({{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = {{\rm{V}}_{{\rm{dd}}}}{\rm{ \times }}\frac{{{\rm{C\% }}}}{{{\rm{100\% }}}}\)
Lời giải chi tiết:
\({{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = {\rm{500 \times }}\frac{{{\rm{5\% }}}}{{{\rm{100\% }}}} = 25{\rm{ (mL)}}\)
→ Chọn B .
24.19
Cho các chất sau: H 2 O (1), C 2 H 5 OH (2), C 6 H 5 OH (3), CH 3 COOH (4).
Độ linh động của nguyên tử hydrogen trong nhóm -OH tăng dần theo thứ tự là
A. (1) < (2) < (3) < (4). B. (1) < (2) < (4) < (3).
C. (2) < (1) < (3) < (4). D. (2) < (1) < (4) < (3).
Phương pháp giải:
Độ linh động của nguyên tử hydrogen trong nhóm –OH càng lớn, phân tử càng có tính acid mạnh.
Tính acid theo thứ tự tăng dần: alcohol < nước < phenol < carboxylic acid.
Lời giải chi tiết:
Độ linh động của nguyên tử hydrogen trong nhóm -OH tăng dần theo thứ tự là
C 2 H 5 OH (2), H 2 O (1), C 6 H 5 OH (3), CH 3 COOH (4).
→ Chọn C .
24.20
Dung dịch acetic acid phản ứng được với tất cả các chất trong dãy nào sau đây?
A. Cu, NaOH, NaCl. B. Zn, CuO, NaCl.
C. Zn, CuO, HCl. D. Zn, NaOH, CaCO 3 .
Phương pháp giải:
Carboxylic acid có tính acid yếu:
+ Làm quỳ tím hóa đỏ.
+ Tác dụng với kim loại đứng trước hydrogen trong dãy hoạt động hóa học, giải phóng khí hydrogen.
+ Tác dụng với base, oxide base.
+ Tác dụng với một số muối.
Lời giải chi tiết:
Acetic acid là acid yếu hơn hydrochloric acid nên acetic acid không phản ứng được với muối NaCl. Acetic acid là acid không phản ứng được với HCl.
Dung dịch acetic acid phản ứng được với Zn, NaOH, CaCO 3 .
→ Chọn D .
24.21
Để loại bỏ lớp cặn màu trắng trong ấm đun nước, người ta có thể dùng dung dịch nào sau đây?
A. Giấm ăn. B. Nước. C. Muối ăn. D. Cồn 70 o .
Phương pháp giải:
Carboxylic acid có tính acid yếu
Lời giải chi tiết:
Để loại bỏ lớp cặn màu trắng trong ấm đun nước, người ta có thể dùng dung dịch giấm ăn.
→ Chọn A .
24.22
Hai chất X và Y có cùng công thức phân tử C 3 H 4 O 2 . Cho X tác dụng với CaCO 3 thấy có bọt khí thoát ra, còn Y có thể tham gia phản ứng tráng bạc. Công thức của X và Y lần lượt là
A. CH 2 =CHCOOH, OHC-CH 2 -CHO. B. CH 2 =CH-COOH, CH≡C-O-CH 2 OH.
C. HOOC-CH=CH 2 , OHC-CH 2 -CHO. D. HOOC-CH=CH 2 , CH≡C-O-CH 2 OH.
Phương pháp giải:
Carboxylic acid có tính acid yếu.
Aldehyde có phản ứng tráng bạc
Lời giải chi tiết:
Cho X tác dụng với CaCO 3 thấy có bọt khí thoát ra, chứng tỏ X là carboxylic acid, X là CH 2 =CHCOOH.
2 CH 2 =CHCOOH + CaCO 3 → 2(CH 2 =CHCOO) 2 Ca + CO 2 ↑ + H 2 O
Y có thể tham gia phản ứng tráng bạc, chứng tỏ Y có nhóm chức –CHO, Y là OHC-CH 2 -CHO.
\({\rm{OHC}} - {\rm{C}}{{\rm{H}}_{\rm{2}}} - {\rm{CHO}} + 4[{\rm{Ag(N}}{{\rm{H}}_{\rm{3}}}{{\rm{)}}_{\rm{2}}}{\rm{]OH}} \to {}_4{\rm{HNOOCC}}{{\rm{H}}_{\rm{2}}}{\rm{COON}}{{\rm{H}}_4} + 4{\rm{Ag}} + 6{\rm{N}}{{\rm{H}}_{\rm{3}}} + 2{{\rm{H}}_2}{\rm{O}}\)
→ Chọn A .
24.23
Khẳng định nào sau đây không đúng khi nói về đặc điểm của phản ứng ester hoá?
A. Phản ứng ester hoá là phản ứng thuận nghịch.
B. Phản ứng ester hoá là phản ứng một chiều.
C. Phản ứng ester hoá luôn có hiệu suất < 100%.
D. Phản ứng ester hoá giữa acid và alcohol thường dùng xúc tác là H 2 SO 4 đặc.
Phương pháp giải:
Phản ứng ester hóa là phản ứng giữa alcohol và carboxylic acid:
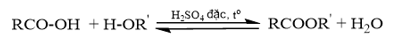
Lời giải chi tiết:
Phản ứng ester hóa là phản ứng là phản ứng thuận nghịch, do đó khẳng định B không đúng.
→ Chọn B .
24.24
Sữa chua được lên men từ sữa bột, sữa bò, sữa dê,... Sữa chua tốt cho hệ tiêu hoá. Vị chua trong sữa chua tạo bởi acid nào sau đây?
A. Formic acid. B. Acetic acid. C. Lactic acid. D. Benzoic acid.
Phương pháp giải:
Trong sữa chua lên men chứa lactic acid.
Lời giải chi tiết:
Vị chua trong sữa chua tạo bởi lactic acid.
→ Chọn C .
24.25
Nhiều acid hữu cơ tạo nên vị chua của các loại trái cây. Ví dụ: trong quả táo có chứa malic acid; trong quả nho, quả me có tartric acid; trong quả chanh, cam có citric acid. Lấy cùng 1 mol các acid trên cho phản ứng với dung dịch Na 2 CO 3 dư, acid nào tạo được thể tích khí lớn nhất? Viết phương trình hoá học, biết công thức cấu tạo của các acid trên là
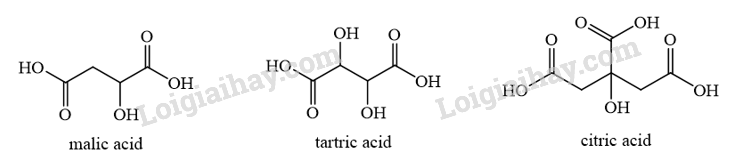
Phương pháp giải:
Carboxylic acid phản ứng với Na 2 CO 3 tạo muối. H trong chức –COOH bị thay bởi Na, ngoài ra sản phẩm còn có H 2 O và CO 2 .
Lời giải chi tiết:
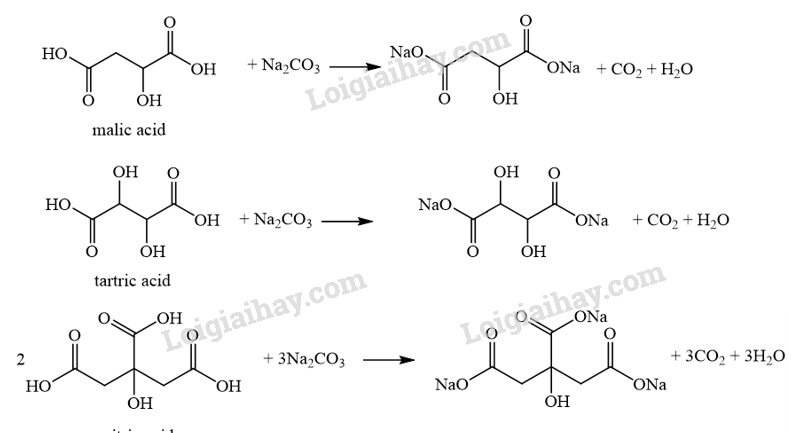
24.26
Hai thí nghiệm được mô tả như hình sau:

Nước vôi trong trong ống nghiệm nào nhanh bị đục hơn? Giải thích và viết phương trình hoá học.
Phương pháp giải:
Acetic acid là acid yếu hơn hydrochloric acid, do đó khi cho hai dung dịch acid này có cùng nồng độ phản ứng với cùng một chất, phản ứng của hydrochloric acid xảy ra nhanh hơn.
Lời giải chi tiết:
Ống nghiệm chứa dung dịch HCl nhanh bị đục hơn do HCl là acid mạnh còn acetic acid là acid yếu.
Phương trình hoá học xảy ra:
\(\begin{array}{l}{\rm{2HCl + CaC}}{{\rm{O}}_{\rm{3}}}{\rm{ }} \to {\rm{ CaC}}{{\rm{l}}_{\rm{2}}}{\rm{ + C}}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}\\{\rm{2C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH + CaC}}{{\rm{O}}_{\rm{3}}}{\rm{ }} \to {\rm{ (C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{)}}_{\rm{2}}}{\rm{Ca + C}}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}\\{\rm{C}}{{\rm{O}}_{\rm{2}}}{\rm{ + Ca(OH}}{{\rm{)}}_{\rm{2}}}{\rm{ }} \to {\rm{ CaC}}{{\rm{O}}_{\rm{3}}} \downarrow {\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}\end{array}\)
24.27
Nhựa PET là một loại polyester được ứng dụng rộng rãi làm chai nhựa, hộp đựng, to sợi,... PET (polyethylene terephthalate) được tổng hợp từ phản ứng ester hoá terephtalic acid và ethylenglycol theo phản ứng sau:
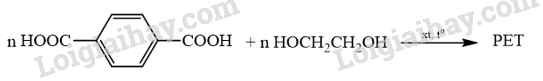
Xác định công thức cấu tạo của PET.
Phương pháp giải:
Phản ứng trùng ngưng, còn được biết đến là phản ứng đồng trùng ngưng, là một quá trình hóa học quan trọng trong đó các monomer, các đơn vị cơ bản chứa các nhóm chất có khả năng tham gia vào phản ứng hóa học, được kết hợp để tạo ra các phân tử polymer dài hơn.
Lời giải chi tiết:
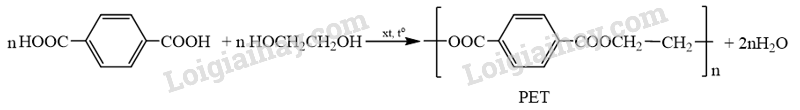
24.28
Đồ thị hình bên mô tả sự phụ thuộc giá trị nhiệt độ sôi vào số nguyên tử carbon của bốn loại hợp chất là alkane, alcohol, aldehyde và carboxylic acid. Đồ thị A, B, C, D lần lượt tương ứng với các loại hợp chất là
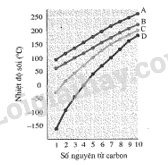
A. alkane, alcohol, aldehyde, carboxylic acid.
B. alcohol, carboxylic acid, aldehyde, alkane.
C. carboxylic acid, aldehyde, alcohol, alkane.
D. carboxylic acid, alcohol, aldehyde, alkane.
Phương pháp giải:
Với các hợp chất có khối lượng phân tử tương đương:
Thứ tự tăng dần về nhiệt độ sôi của các chất là: alkane < aldehyde < alcohol < carboxylic acid.
Lời giải chi tiết:
A có nhiệt độ sôi cao nhất, do đó A là carboxylic acid.
Tiếp theo, B là alcohol, C là aldehyde.
D có nhiệt độ sôi thấp nhất, D là alkane.
→ Chọn D .
24.29
Một loại giấm ăn có chứa hàm lượng 4,5% acetic acid về thể tích.
a) Tính khối lượng acetic acid trong một can giấm có dung tích 5L.
b) Tính thể tích dung dịch NaOH 2M cần để trung hoà hết lượng giấm trên, biết khối lượng riêng của acetic acid là D = 1,05 g/mL.
Phương pháp giải:
Tính chất đặc trưng của carboxylic acid là tính acid (làm đổi màu quỳ tím, tác dụng với kim loại, base, oxide base, muối) và phản ứng ester hóa.
Lời giải chi tiết:
a) Thể tích của acetic acid trong 5L giấm ăn:
\({{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = {\rm{5000 \times }}\frac{{{\rm{4,5\% }}}}{{{\rm{100\% }}}} = 225{\rm{ (mL)}}\)
Khối lượng của acetic acid trong 5L giấm ăn:
\({{\rm{m}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = 225 \times 1,05 = 236,25{\rm{ (g)}}\)
b) \({{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = \frac{{236,25}}{{60}}{\rm{ = 3,9375 (mol)}}\)
Phương trình hóa học: \({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}} + {\rm{NaOH}} \to {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COONa}} + {{\rm{H}}_{\rm{2}}}{\rm{O}}\)
\(\begin{array}{l} \Rightarrow {{\rm{n}}_{{\rm{NaOH}}}} = {{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = 3,9375{\rm{ (mol)}}\\ \Rightarrow {{\rm{V}}_{{\rm{NaOH}}}} = \frac{{3,9375}}{2} \approx 1,969{\rm{ (L)}}\end{array}\)
24.30
Cho 4,32 g acid hữu cơ X đơn chức tác dụng hết với Na 2 CO 3 , thu được 5,64 g muối của acid hữu cơ. Xác định công thức cấu tạo của X.
Phương pháp giải:
Sử dụng phương pháp tăng giảm khối lượng để tìm được số mol acid, từ đó tính M của acid và suy ra công thức cấu tạo.
Lời giải chi tiết:
Gọi công thức tổng quát của X là RCOOH.
Phương trình hóa học: \({\rm{2RCOOH}} + {\rm{N}}{{\rm{a}}_{\rm{2}}}{\rm{C}}{{\rm{O}}_{\rm{3}}} \to 2{\rm{RCOONa}} + {\rm{C}}{{\rm{O}}_{\rm{2}}} + {{\rm{H}}_{\rm{2}}}{\rm{O}}\)
Ta có: \({{\rm{n}}_{{\rm{RCOOH}}}}{\rm{ = }}{{\rm{n}}_{{\rm{RCOONa}}}}{\rm{ = a (mol)}}\)
Theo phương pháp tăng giảm khối lượng:
\(\begin{array}{l}{\rm{ }}{{\rm{m}}_{{\rm{RCOONa}}}}{\rm{ }} - {\rm{ }}{{\rm{m}}_{{\rm{RCOOH}}}}{\rm{ = 5,64 }} - {\rm{ 4,32}}\\ \Leftrightarrow ({\rm{R}} + 12 + 16 \times 2 + 23){\rm{a}} - ({\rm{R}} + 12 + 16 \times 2 + 1){\rm{a = 1,32}}\\ \Leftrightarrow ({\rm{R}} + 67){\rm{a}} - ({\rm{R}} + 45){\rm{a = 1,32}}\\ \Leftrightarrow {\rm{Ra}} + 67{\rm{a}} - {\rm{Ra}} - 45{\rm{a = 1,32}}\\ \Rightarrow {\rm{a}} = \frac{{1,32}}{{67 - 45}} = 0,06{\rm{ (mol)}}\\ \Rightarrow {{\rm{M}}_{{\rm{RCOOH}}}} = \frac{{4,32}}{{0.06}} = 72{\rm{ (g/mol)}}\\ \Rightarrow {{\rm{M}}_{\rm{R}}} = 72 - 45 = 27\end{array}\)
\( \Rightarrow \)R là C 2 H 3 -
Công thức cấu tạo của X là \({\rm{C}}{{\rm{H}}_{\rm{2}}} = {\rm{CH}} - {\rm{COOH}}\)
24.31
Để xác định hàm lượng của acetic acid trong một loại giấm ăn, một học sinh pha loãng loại giấm ăn đó mười lần rồi tiến hành chuần độ 10 mL giấm ăn sau pha loãng bằng dung dịch NaOH 0,1M, thu được kết quả như bảng sau:
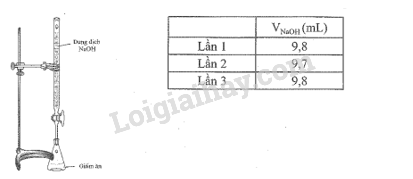
Tính hàm lượng % về thể tích acetic acid có trong loại giấm đó, biết khối lượng riêng của acetic acid là D = 1,05 g/mL, giả thiết trong thành phần giấm ăn chỉ có acetic acid phản ứng với NaOH.
Phương pháp giải:
Tính số mol của NaOH từ đó tính số mol của acetic acid theo phương trình hóa học và tính thể tích acetic acid.
Lời giải chi tiết:
\(\begin{array}{l}{\overline {\rm{V}} _{{\rm{NaOH}}}} = \frac{{9,8 + 9,7 + 9,8}}{3} \approx 9,767{\rm{ (mL)}}\\ \Rightarrow {{\rm{n}}_{{\rm{NaOH}}}} = 9,767 \times {10^{ - 3}} \times 0,1 = 9,767 \times {10^{ - 4}}({\rm{mol}})\end{array}\)
Xét phương trình hóa học: \({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}} + {\rm{NaOH}} \to {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COONa}} + {{\rm{H}}_{\rm{2}}}{\rm{O}}\)
\(\begin{array}{l}{{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = }}{{\rm{n}}_{{\rm{NaOH}}}}{\rm{ = }}9,767 \times {10^{ - 4}}({\rm{mol}})\\ \Rightarrow {{\rm{m}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = }}9,767 \times {10^{ - 4}} \times 60 = 0,0586{\rm{ (g)}}\\ \Rightarrow {{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = }}\frac{{0,0586}}{{1,05}} = 0,0558{\rm{ (mL)}}\end{array}\)
Hàm lượng acetic acid trong 10 mL giấm ăn: \(\frac{{0,0558}}{{10}} \times 100\% = 0,558\% \)
Vì loại giấm ăn này đã được pha loãng 10 lần trước khi đem đi chuẩn độ, nên hàm lượng acetic acid trong giấm ăn ban đầu là 5,58%.
24.32
Citric acid có nhiều trong quả chanh, có công thức phân tử là C 6 H 8 O 7 . Cho 1 mol citric acid phản ứng với Na 2 CO 3 thì thấy tỉ lệ mol cần thiết là 2: 3. Xác định công thức cấu tạo của citric acid biết rằng citric acid mạch chính chứa 5C, có chứa các nhóm chức –COOH, -OH và có cấu tạo đối xứng.
Phương pháp giải:
Một nhóm chức –COOH phản ứng với NaOH theo tỉ lệ 1:1.
Lời giải chi tiết:
Citric acid phản ứng với Na 2 CO 3 theo tỉ lệ 2 : 3
⇒ có 3 nhóm –COOH. Do vậy citric acid có 1 nhóm –OH.
Citric acid mạch chính có 5C và có cấu tạo đối xứng nên công thức cấu tạo của citric acid là:
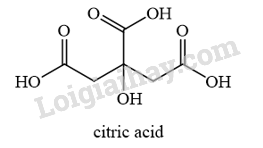
24.33
Trộn 20 mL ethanol với 20 mL acetic acid, thêm 10 mL H 2 SO 4 đặc rồi tiến hành phản ứng ester hoá. Sau một thời gian, thu được 17,6 g ester. Tính hiệu suất phản ứng ester, biết khối lượng riêng của ethanol và acetic acid lần lượt là 0,789 g/mL và 1,05 g/mL.
Phương pháp giải:
Phản ứng ester hóa là phản ứng giữa alcohol và carboxylic acid:

Lời giải chi tiết:
\(\begin{array}{l}{{\rm{m}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = 20 \times 0,789 = 15,78{\rm{ (g)}} \Rightarrow {{\rm{n}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = \frac{{15,78}}{{46}} \approx 0,343{\rm{ (mol)}}\\{{\rm{m}}_{{\rm{C}}{{\rm{H}}_3}{\rm{COOH}}}} = 20 \times 1,05 = 21{\rm{ (g)}} \Rightarrow {{\rm{n}}_{{\rm{C}}{{\rm{H}}_3}{\rm{COOH}}}} = \frac{{21}}{{60}} = 0,35{\rm{ (mol)}}\end{array}\)
Xét phương trình phản ứng:
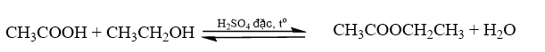
Ta có: \(\frac{{{{\rm{n}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}}}}{1} < \frac{{{{\rm{n}}_{{\rm{C}}{{\rm{H}}_3}{\rm{COOH}}}}}}{1}(0,343 < 0,35)\)
Do đó, C 2 H 5 OH hết, hiệu suất tính theo C 2 H 5 OH.
\( \Rightarrow {{\rm{n}}_{{\rm{ester}}}}_{{\rm{(LT)}}} = {{\rm{n}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = 0,343{\rm{ (mol)}}\)
Ta có: \({{\rm{n}}_{{\rm{ester}}}}_{{\rm{(TT)}}} = \frac{{17,6}}{{88}}{\rm{ = 0,2 (mol)}}\)
\( \Rightarrow {\rm{H}} = \frac{{0,2}}{{0,343}} \times {\rm{100\% }} \approx {\rm{58,3\% }}\)