Bài 20. Alcohol trang 69, 70, 71, 72, 73, 74 SBT Hóa 11 Kết nối tri thức
Công thức tổng quát của alcohol no, đơn chức, mạch hở là A. CnH2n-5OH. B. CnH2n(OH)2. C. CnH2n-1OH. D. CnH2n+1OH.
20.1
Công thức tổng quát của alcohol no, đơn chức, mạch hở là
A. C n H 2n-5 OH. B. C n H 2n (OH) 2 . C. C n H 2n-1 OH. D. C n H 2n+1 OH.
Phương pháp giải:
Alcohol no, đơn chức, mạch hở trong phân tử có một nhóm – OH liên kết với gốc alkyl, có công thức tổng quát là C n H 2n+1 OH (n ≥ 1). Ví dụ: CH 3 OH; C 2 H 5 OH …
Lời giải chi tiết:
Công thức tổng quát của alcohol no, đơn chức, mạch hở là C n H 2n+1 OH.
→ Chọn D .
20.2
Số đồng phân cấu tạo alcohol có công thức C 4 H 9 OH là
A. 2. B. 3. C. 4. D. 5.
Phương pháp giải:
Alcohol no, đơn chức, mạch hở trong phân tử có một nhóm – OH liên kết với gốc alkyl, có công thức tổng quát là C n H 2n+1 OH (n ≥ 1). Ví dụ: CH 3 OH; C 2 H 5 OH …
Lời giải chi tiết:
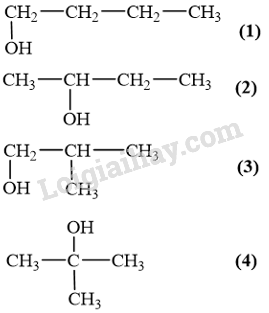
Số đồng phân cấu tạo alcohol có công thức C 4 H 9 OH là 4.
→ Chọn C .
20.3
Chất nào sau đây là alcohol bậc II?
A. propan-1-ol. B. propan-2-ol.
C. 2-methylpropan-1-ol. D. 2-methylpropan-2-ol.
Phương pháp giải:
Bậc của alcohol là bậc của nguyên tử carbon liên kết với nhóm hydroxy. Do đó, ta có alcohol bậc I, alcohol bậc II và alcohol bậc III.
Lời giải chi tiết:
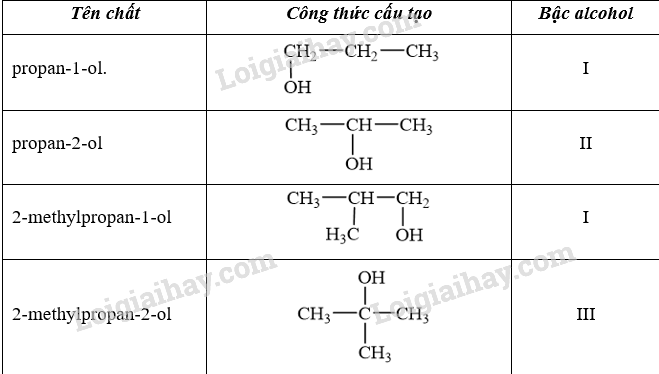
Propan-2-ol là alcohol bậc II.
→ Chọn B .
20.4
Cho alcohol có công thức cấu tạo sau:
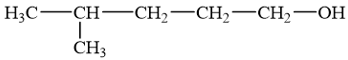
Tên theo danh pháp thay thế của alcohol đó là
A. 4-methylpentan-1-ol. B. 2-methylbutan-3-ol.
C. 3-methylbutan-2-ol. D. 1,1-dimethylpropan-3-ol.
Phương pháp giải:
Tên theo danh pháp thay thế của monoalcohol: Tên hydrocarbon (bỏ e ở cuối) - vị trí nhóm (OH) - ol
Lời giải chi tiết:
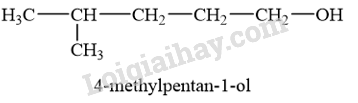
→ Chọn A .
20.5
Nhiều vụ ngộ độc rượu do sử dụng rượu được pha chế từ cồn công nghiệp có lẫn methanol. Công thức phân tử của methanol là
A. CH 3 OH. B. C 2 H 5 OH. C. C 3 H 7 OH. D. C 2 H 4 (OH) 2 .
Phương pháp giải:
Methanol là alcohol no, hở, đơn, phân tử có 1 carbon.
Lời giải chi tiết:
Công thức phân tử của methanol là CH 3 OH.
→ Chọn A .
20.6
Cho các hợp chất hữu cơ sau: (1) C 3 H 8 ; (2) CH 3 Cl; (3) C 2 H 5 OH; (4) CH 3 OH.
Thứ tự giảm dần nhiệt độ sôi của các chất trên là
A. (1) > (2) > (3) > (4). B. (1) > (4) > (2) > (3).
C. (3) > (4) > (2) > (1). D. (4) > (2) > (1) > (3).
Phương pháp giải:
Nhiệt độ sôi của các alcohol tăng khi phân tử khối tăng.
Alcohol có nhiệt độ sôi cao hơn các hydrocarbon, dẫn xuất halogen có phân tử khối tương đương.
Nhiệt độ sôi của các dẫn xuất halogen cao hơn các hydrocarbon có phân tử khối tương đương.
Lời giải chi tiết:
Thứ tự giảm dần nhiệt độ sôi: (3) C 2 H 5 OH; (4) CH 3 OH; (2) CH 3 Cl; (1) C 3 H 8 .
→ Chọn C .
20.7
Để pha chế một loại cồn sát trùng sử dụng trong y tế, người ta cho 700 mL ethanol nguyên chất vào bình định mức rồi thêm nước cất vào, thu được 1000 mL cồn. Hồn hợp trên có độ cồn là
A. 17 o . B. 7 o . C. 70 o . D. 170 o .
Phương pháp giải:
Độ cồn (độ rượu) là số ml rượu nguyên chất có trong 100 mL rượu và nước.
Gọi a là độ cồn của dung dịch ethanol: \({\rm{a}} = \frac{{{{\rm{V}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}}}}{{{{\rm{V}}_{{\rm{dd }}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}}}} \times 100\)
Lời giải chi tiết:
\({\rm{a}} = \frac{{{\rm{700}}}}{{{\rm{1000}}}} \times 100 = {70^{\rm{o}}}\)
→ Chọn C .
20.8
Số hợp chất hữu cơ có công thức phân tử C 3 H 8 O phản ứng được với Na là
A. 1. B. 2. C. 3. D. 4.
Phương pháp giải:
Liên kết O – H phân cực nên trong một số phản ứng, nguyên tử hydrogen trong nhóm hydroxy có thể bị thay thế. Alcohol phản ứng với các kim loại mạnh như sodium, potassium giải phóng khí hydrogen:
2R – OH + 2Na → 2RONa + H 2
Lời giải chi tiết:
Các đồng phân alcohol có công thức phân tử C 3 H 8 O phản ứng được với Na:
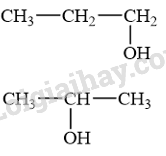
→ Chọn B .
20.9
Cho phản ứng hoá học sau:
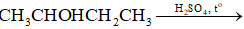
Sản phẩm chính theo quy tắc Zaitsev trong phản ứng trên là
A. but-1-ene. B. but-2-ene. C. but-1-yne. D. but-2-yne.
Phương pháp giải:
Khi cho hơi alcohol no, đơn chức, mạch hở đi qua bột Al 2 O 3 nung nóng hoặc đun alcohol với H 2 SO 4 đặc, H 3 PO 4 đặc, alcohol bị tách nước tạo thành alkene.
Phản ứng tách nước của alcohol tạo alkene ưu tiên theo quy tắc tách Zaitsev: Trong phản ứng tách nước của alcohol, nhóm – OH bị tách ưu tiên cùng với nguyên tử hydrogen ở carbon bên cạnh có bậc cao hơn.
Lời giải chi tiết:
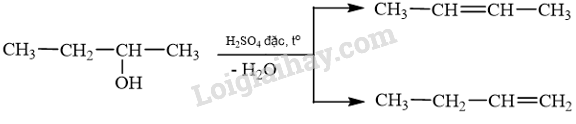
Sản phẩm chính theo quy tắc Zaitsev trong phản ứng trên là but-2-ene.
→ Chọn B .
20.10
Oxi hoá propan-2-ol bằng CuO nung nóng, thu được sản phẩm nào sau đây?
A. CH 3 CHO. B. CH 3 CH 2 CHO. C. CH 3 COCH 3 . D. CH 3 COOH.
Phương pháp giải:
Oxi hoá không hoàn toàn alcohol bằng cách đun nóng alcohol với CuO.
+ Các alcohol bậc I bị oxi hóa không hoàn toàn tạo thành aldehyde.
+ Các alcohol bậc II bị oxi hóa không hoàn toàn tạo thành ketone.
+ Trong điều kiện trên, alcohol bậc III không phản ứng.
Lời giải chi tiết:
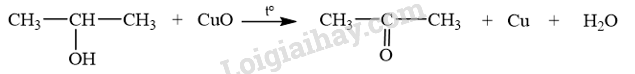
Oxi hoá propan-2-ol bằng CuO nung nóng, thu được CH 3 COCH 3 .
→ Chọn C .
20.11
Thuốc thử Cu(OH) 2 dùng để nhận biết alcohol nào sau đây?
A. Alcohol bậc I. B. Alcohol bậc II.
C. Alcohol bậc III. D. Alcohol đa chức.
Phương pháp giải:
Các polyalcohol có các nhóm – OH liền kề như ethylene glycol, glycerol có thể tác dụng với copper(II) hydroxide tạo thành dung dịch màu xanh lam đậm. Vì vậy, phản ứng này có thể dùng để nhận biết các polyalcohol có các nhóm – OH liền kề.
Lời giải chi tiết:
Thuốc thử Cu(OH) 2 dùng để nhận biết alcohol đa chức.
→ Chọn D .
20.12
Khi đốt cháy hoàn toàn ethanol, thu được tỉ lệ mol \({{\rm{n}}_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}}:{{\rm{n}}_{{{\rm{H}}_{\rm{2}}}{\rm{O}}}}\)
A. 1 : 1. B. 1 : 2. C. 2 : 3. D. 3 : 2.
Phương pháp giải:
Các alcohol có thể bị đốt cháy trong không khí tạo thành carbon dioxide, hơi nước và toả nhiệt.
Lời giải chi tiết:
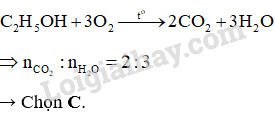
20.13
Chất nào sau đây dùng để điều chế ethanol theo phương pháp sinh hoá?
A. Ethylene. B. Acetylene. C. Methane. D. Tinh bột.
Phương pháp giải:

Lời giải chi tiết:
Tinh bột được dùng để điều chế ethanol theo phương pháp sinh hoá.
→ Chọn D .
20.14
Để phân biệt cồn 90 o và cồn tuyệt đối (ethanol nguyên chất), có thể dùng hoá chất nào sau đây?
A. Na. B. CuSO 4 khan. C. CuO, t o . D. Cu(OH) 2 .
Phương pháp giải:
CuSO 4 là đồng khan, tồn tại dưới dạng bột màu trắng.
Đặc tính: Hút ẩm mạnh, để trong không khí dễ hấp thụ hơi nước tạo thành CuSO 4 .5H 2 O có màu xanh lam. Chính vì thế đồng khan được sử dụng để phát hiện nước có lẫn trong các hợp chất hữu cơ.
Lời giải chi tiết:
Dùng CuSO 4 khan để phân biệt cồn 90 o và cồn tuyệt đối. Nhỏ cồn 90 o và cồn tuyệt đối vào hai mẫu chứa CuSO 4 khan.
Cồn 90 o làm bột CuSO 4 khan chuyển thành màu xanh lam. Mẫu bột CuSO 4 khan không đổi màu khi nhỏ cồn tuyệt đối vào.
→ Chọn B .
20.15
Hai ancol nào sau đây cùng bậc?
A. Methanol và ethanol. B. Propan-1-ol và propan-2-ol.
C. Ethanol và propan-2-ol. D. Propan-2-ol và 2-methylpropan-2-ol.
Phương pháp giải:
Bậc của alcohol là bậc của nguyên tử carbon liên kết với nhóm hydroxy. Do đó, ta có alcohol bậc I, alcohol bậc II và alcohol bậc III.
Lời giải chi tiết:
Methanol và ethanol đều là alcohol bậc I.
Propan-1-ol là alcohol bậc I và propan-2-ol là alcohol bậc II.
Ethanol là alcohol bậc I và propan-2-ol là alcohol bậc II.
Propan-2-ol là alcohol bậc II và 2-methylpropan-2-ol là alcohol bậc III.
→ Chọn A .
20.16
Alcohol CH 3 CH=CHCH 2 OH có danh pháp thay thế là
A. but-2-en-4-ol. B. but-2-en-1-ol.
C. 4-hydroxybut-2-ene. D. 1-hydroxybut-2-ene.
Phương pháp giải:
Tên theo danh pháp thay thế của monoalcohol: Tên hydrocarbon (bỏ e ở cuối) - vị trí nhóm (OH) - ol
Lời giải chi tiết:
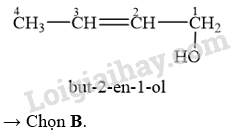
20.17
Một học sinh sau khi tiến hành thí nghiệm thì vẫn còn dư mẩu Na. Để tiêu huỷ mẩu Na dư này một cách an toàn, học sinh đó nên cho mẩu Na vào
A. nước. B. cồn 96 o . C. thùng rác. D. dầu hoả.
Phương pháp giải:
Liên kết O – H phân cực nên trong một số phản ứng, nguyên tử hydrogen trong nhóm hydroxy có thể bị thay thế. Alcohol phản ứng với các kim loại mạnh như sodium, potassium giải phóng khí hydrogen:
2R – OH + 2Na → 2RONa + H 2
Lời giải chi tiết:
Na phản ứng mãnh liệt với nước. Do đó không tiêu hủy Na bằng nước.
Na phản ứng êm dịu với cồn 96 o theo phản ứng: \(2{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{--OH }} + {\rm{ }}2{\rm{Na }} \to {\rm{ }}2{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{ONa }} + {\rm{ }}{{\rm{H}}_{\rm{2}}}\).
\( \Rightarrow \)Do đó có thể tiêu hủy Na bằng cồn 96 o .
Na là kim loại hoạt động mạnh, không bỏ Na vào thùng rác, dễ có nguy cơ gây cháy, nổ.
Na không phản ứng với dầu hỏa, bỏ Na vào dầu hỏa là cách bảo quản Na, không phải cách tiêu hủy.
→ Chọn B .
20.18
Một chai rượu gạo có thể tích 750 mL và có độ rượu là 40 o . Số mL ethanol nguyên chất (khan) có trong chai rượu đó là
A. 18,75 mL. B. 300 mL. C. 400 mL. D. 750 mL.
Phương pháp giải:
Độ cồn (độ rượu) là số ml rượu nguyên chất có trong 100 mL rượu và nước.
Gọi a là độ cồn của dung dịch ethanol: \({\rm{a}} = \frac{{{{\rm{V}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}}}}{{{{\rm{V}}_{{\rm{dd }}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}}}} \times 100\)
Lời giải chi tiết:
\({{\rm{V}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = 750 \times \frac{{40}}{{100}} = 300{\rm{ (mL)}}\)
→ Chọn B .
20.19
Xăng E5 chứa 5% thể tích ethanol hiện đang được sử dụng phổ biến ở nước ta để thay thế một phần xăng thông thường. Một người đi xe máy mua 2 L xăng E5 để đổ vào bình chứa nhiên liệu. Thể tích ethanol có trong lượng xăng trên là
A. 50 mL. B. 92 mL. C. 46 mL. D. 100 mL.
Phương pháp giải:
Xăng E5 chứa 5% thể tích ethanol.
Lời giải chi tiết:
\({{\rm{V}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = 2 \times \frac{{5\% }}{{100\% }} = 0,1{\rm{ (L) = 100 (mL)}}\)
→ Chọn D .
20.20
Cho các alcohol sau:
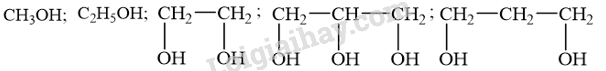
Số alcohol không hoà tan được Cu(OH) 2 là
A. 1. B. 2. C. 3. D. 4.
Phương pháp giải:
Các polyalcohol có các nhóm – OH liền kề như ethylene glycol, glycerol có thể tác dụng với copper(II) hydroxide tạo thành dung dịch màu xanh lam đậm. Vì vậy, phản ứng này có thể dùng để nhận biết các polyalcohol có các nhóm – OH liền kề.
Lời giải chi tiết:
Các alcohol không có các nhóm – OH liền kề nhau không hòa tan được Cu(OH) 2 :
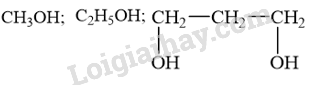
→ Chọn C .
20.21
Nhận xét nào sau đây không đúng?
A. Oxi hoá không hoàn toàn alcohol bậc I, thu được aldehyde.
B. Oxi hoá hoàn toàn alcohol bậc I, thu được aldehyde.
C. Oxi hoá alcohol bậc II, thu được ketone.
D. Alcohol bậc III không bị oxi hoá bởi tác nhân thông thường.
Phương pháp giải:
Oxi hoá không hoàn toàn alcohol bằng cách đun nóng alcohol với CuO:
+ Các alcohol bậc I bị oxi hóa không hoàn toàn tạo thành aldehyde.
+ Các alcohol bậc II bị oxi hóa không hoàn toàn tạo thành ketone.
+ Trong điều kiện trên, alcohol bậc III không phản ứng.
Lời giải chi tiết:
Nhận xét B sai vì oxi hóa hoàn toàn alcohol bậc I, thu được CO 2 và H 2 O.
→ Chọn B .
20.22
Sản phẩm chính thu được khi tách nước từ 3-methylbutan-2-ol là
A. 3-metylbut-1-ene. B. 2-methylbut-2-ene.
C. 3-methylbut-2-ene. D. 2-methylbut-3-ene.
Phương pháp giải:
Khi cho hơi alcohol no, đơn chức, mạch hở đi qua bột Al 2 O 3 nung nóng hoặc đun alcohol với H 2 SO 4 đặc, H 3 PO 4 đặc, alcohol bị tách nước tạo thành alkene.
Phản ứng tách nước của alcohol tạo alkene ưu tiên theo quy tắc tách Zaitsev: Trong phản ứng tách nước của alcohol, nhóm – OH bị tách ưu tiên cùng với nguyên tử hydrogen ở carbon bên cạnh có bậc cao hơn.
Lời giải chi tiết:
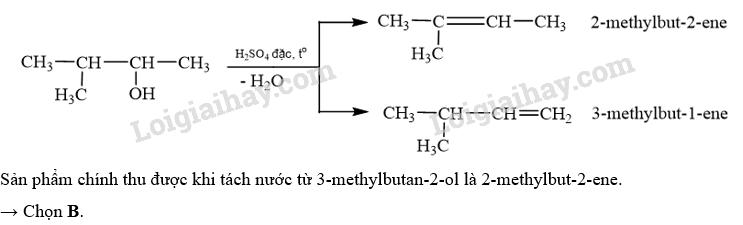
20.23
Oxi hoá alcohol nào sau đây thu được sản phẩm là ketone?
A. C 2 H 5 OH. B. CH 3 CH 2 CH 2 OH.
C. CH 3 CH(OH)CH 3 . D. (CH 3 ) 2 C(OH)CH 3 .
Phương pháp giải:
Oxi hoá không hoàn toàn alcohol bằng cách đun nóng alcohol với CuO.
+ Các alcohol bậc I bị oxi hóa không hoàn toàn tạo thành aldehyde.
+ Các alcohol bậc II bị oxi hóa không hoàn toàn tạo thành ketone.
+ Trong điều kiện trên, alcohol bậc III không phản ứng.
Lời giải chi tiết:
Oxi hóa CH 3 CH(OH)CH 3 thu được sản phẩm là ketone.

→ Chọn C .
20.24
Phương pháp nào sau đây dùng để sản xuất ethanol sinh học?
A. Cho hỗn hợp khí ethylene và hơi nước đi qua tháp chứa H 3 PO 4 .
B. Cộng nước vào ethylene với xúc tác là H 2 SO 4 .
C. Lên men tinh bột.
D. Thuỷ phân dẫn xuất C 2 H 5 Br trong môi trường kiềm.
Phương pháp giải:

Lời giải chi tiết:
Phương pháp lên men tinh bột dùng để sản xuất ethanol sinh học.
→ Chọn C .
20.25
Cho dãy chuyển hoá sau:
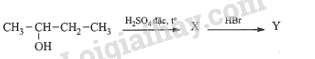
Biết X và Y đều là sản phẩm chính, công thức cấu tạo của X, Y lần lượt là
A. CH 3 CH=CHCH 3 và CH 3 CH 2 CHBrCH 3 .
B. C 4 H 9 -O-C 4 H 9 và CH 3 CH 2 CHBrCH 3 .
C. CH 2 =CHCH 2 CH 3 và CH 3 CH 2 CHBrCH 3 .
D. CH 2 =CHCH 2 CH 3 và CH 3 CH 2 CH 2 CH 2 Br.
Phương pháp giải:
Phản ứng tách nước của alcohol tạo alkene ưu tiên theo quy tắc tách Zaitsev: Trong phản ứng tách nước của alcohol, nhóm – OH bị tách ưu tiên cùng với nguyên tử hydrogen ở carbon bên cạnh có bậc cao hơn.
Phản ứng cộng acid, cộng nước vào alkyne cũng tuân theo quy tắc Markovnikov: Phản ứng cộng một tác nhân không đối xứng HX như HBr, HCl, HI, HOH, … vào liên kết bội, nguyên tử hydrogen sẽ ưu tiên cộng vào nguyên tử carbon có nhiều hydrogen hơn và X sẽ cộng vào nguyên tử carbon có ít hydrogen hơn.
Lời giải chi tiết:
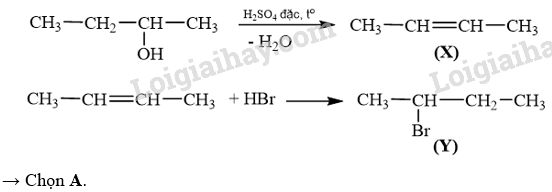
20.26
a) Viết các đồng phân cấu tạo alcohol bậc I có công thức C 5 H 11 OH.
b) Đun nóng một trong các alcohol trên với H 2 SO 4 đặc, thu được alkene có tên gọi là 3-methylbut-1-ene, xác định công thức của alcohol đó.
Phương pháp giải:
a) Alcohol no, đơn chức, mạch hở trong phân tử có một nhóm – OH liên kết với gốc alkyl, có công thức tổng quát là C n H 2n+1 OH (n ≥ 1). Ví dụ: CH 3 OH; C 2 H 5 OH …
Bậc của alcohol là bậc của nguyên tử carbon liên kết với nhóm hydroxy. Do đó, ta có alcohol bậc I, alcohol bậc II và alcohol bậc III.
b) Khi cho hơi alcohol no, đơn chức, mạch hở đi qua bột Al 2 O 3 nung nóng hoặc đun alcohol với H 2 SO 4 đặc, H 3 PO 4 đặc, alcohol bị tách nước tạo thành alkene.
Phản ứng tách nước của alcohol tạo alkene ưu tiên theo quy tắc tách Zaitsev: Trong phản ứng tách nước của alcohol, nhóm – OH bị tách ưu tiên cùng với nguyên tử hydrogen ở carbon bên cạnh có bậc cao hơn.
Lời giải chi tiết:
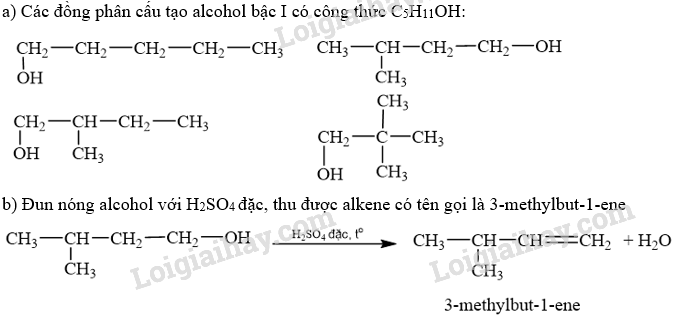
20.27
Một học sinh tiến hành thí nghiệm như sau: Lấy một mẩu nhỏ Na vào cốc chứa ethanol dư, thấy mẩu tan dần và có sủi bọt khí. Sau khi kết thúc phản ứng thấy có kết tủa trắng xuất hiện, thêm một ít nước vào dung dịch sau phản ứng thấy kết tủa tan. Nhỏ vài giọt phenolphtalein vào dung dịch thu được, thấy dung dich chuyển thành màu hồng. Giải thích các hiện tượng trên và viết phương trình hoá học của phản úng xảy ra.
Phương pháp giải:
Liên kết O – H phân cực nên trong một số phản ứng, nguyên tử hydrogen trong nhóm hydroxy có thể bị thay thế. Alcohol phản ứng với các kim loại mạnh như sodium, potassium giải phóng khí hydrogen:
2R – OH + 2Na → 2RONa + H 2
Lời giải chi tiết:
Cho mẫu Na vào cốc chứa ethanol dư, xuất hiện khí H 2 và kết tủa trắng là C 2 H 5 ONa:
\(2{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{--OH }} + {\rm{ }}2{\rm{Na }} \to {\rm{ }}2{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{ONa }} + {\rm{ }}{{\rm{H}}_{\rm{2}}}\)
Khi thêm nước vào kết tủa tan do xảy ra phản ứng: \({{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{ONa}} + {{\rm{H}}_{\rm{2}}}{\rm{O}} \to {{\rm{C}}_{\rm{2}}}{{\rm{H}}_5}{\rm{OH}} + {\rm{NaOH}}\)
Do có NaOH tạo thành làm phenolphtalein chuyển màu hồng.
20.28
Thí nghiệm theo sơ đồ sau đây được dùng để điều chế một lượng nhỏ ethylene trong phòng thí nghiệm.
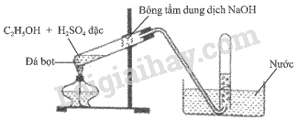
a) Viết phương trình hoá học của phản ứng xảy ra.
b) Tại sao lại dùng phương pháp đẩy nước để thu khí ethylene.
c) Nêu tác dụng của bông tẩm dung dịch NaOH.
d) Đề xuất thí nghiệm để nhận biết khí tạo thành.
Phương pháp giải:
a) Khi cho hơi alcohol no, đơn chức, mạch hở đi qua bột Al 2 O 3 nung nóng hoặc đun alcohol với H 2 SO 4 đặc, H 3 PO 4 đặc, alcohol bị tách nước tạo thành alkene.
b) Có thể thu các khí không tan hoặc ít tan trong nước bằng phương pháp đẩy nước.
c) Dung dịch kiềm phản ứng với các oxide base.
d) Các hydrocarbon không no làm mất màu thuốc tím và nước bromine ở điều kiện thường.
Lời giải chi tiết:
a) Phương trình hóa học:
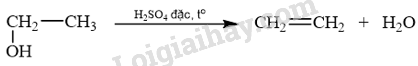
b) Khí ethylene hầu như không tan trong nước nên có thể sử dụng phương pháp đẩy nước để thu khí ethylene.
c) Bông tẩm dung dịch NaOH để hấp thụ các tạp chất tạo thành trong quá trình phản ứng như SO 2 , CO 2 .
d) Dẫn khí thoát ra sục vào ống nghiệm chứa nước bromine hoặc thuốc tím, các ống nghiệm này sẽ mất màu chứng tỏ có khí ethylene tạo thành.
20.29
Tính lượng glucose cần lên men để sản xuất 100 L cồn y tế 70 o , biết hiệu suất của quá trình lên men là 80%, khối lượng riêng của ethanol là 0,789 g/mL.
Phương pháp giải:
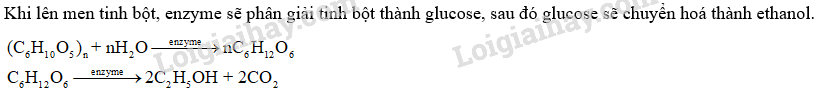
Lời giải chi tiết:
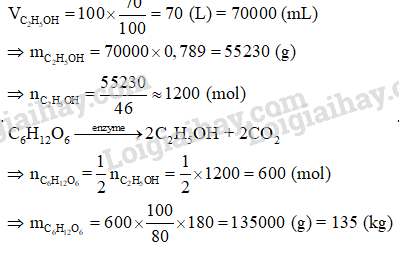
20.30
Một đèn cồn thí nghiệm chứa 100 mL cồn 90 o . Tính nhiệt lượng đèn cồn toả ra khi đốt cháy hết lượng cồn trên, biết khối lượng riêng của ethanol là 0,789 g/mL và nhiệt sinh ra khi đốt cháy 1 mol ethanol là 1371 kJ.mol -1 .
Phương pháp giải:
Độ cồn (độ rượu) là số ml rượu nguyên chất có trong 100 mL rượu và nước.
Gọi a là độ cồn của dung dịch ethanol: \({\rm{a}} = \frac{{{{\rm{V}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}}}}{{{{\rm{V}}_{{\rm{dd }}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}}}} \times 100\)
Lời giải chi tiết:
\(\begin{array}{l}{{\rm{V}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = 100 \times \frac{{90}}{{100}} = 9{\rm{0 (mL)}}\\ \Rightarrow {{\rm{m}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = {\rm{90}} \times 0,789 = 71,01{\rm{ (g)}}\\ \Rightarrow {{\rm{n}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = \frac{{71,01}}{{46}} \approx 1,5437{\rm{ (mol)}}\end{array}\)
Nhiệt sinh ra khi đốt cháy hết lượng cồn trên là
20.31
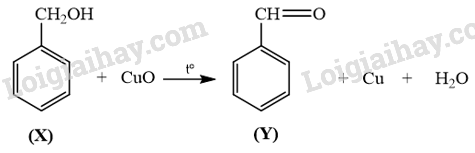
Hợp chất X có tác dụng kháng khuần, chống vi sinh vật kí sinh trên da (chấy, rận,..). X có công thức phân tử C 7 H 8 O và có chứa vòng benzene, phổ IR của X có peak hấp thụ rộng ở vùng 3300 cm -1 . Oxi hoá X bằng CuO nung nóng, thu được hợp chất Y có peak hấp thụ đặc trưng ở khoảng 1700 cm -1 . Xác định công thức cấu tạo của X, Y và viết phương trình hoá học của phản ứng xảy ra.
Phương pháp giải:
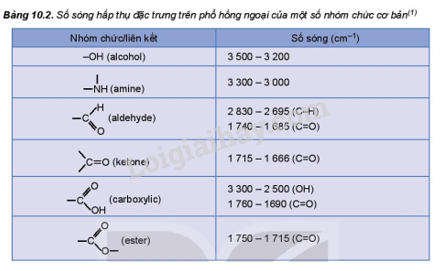
Lời giải chi tiết:
Phổ IR của X có peak hấp thụ rộng ở vùng 3 300 cm -1 : có nhóm –OH.
Phổ IR của Y có peak hấp thụ rộng ở vùng 1 700 cm -1 : có nhóm C=O.
Vậy X là benzyl alcohol, Y là aldehyde benzoic.
20.32
Từ 1 tấn tinh bột ngô có thể sản xuất được bao nhiêu lít xăng E5 (chứa 5% ethanol về thể tích), biết tinh bột ngô chứa 75% tinh bột, hiệu suất chung của cả quá trình điều chế ethanol là 70%, khối lượng riêng của ethanol là 0,789 g/mL.
Phương pháp giải:
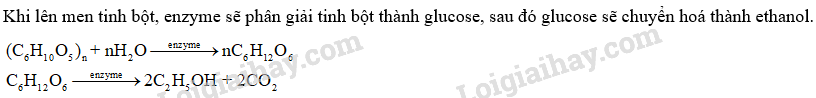
Lời giải chi tiết:
\(\begin{array}{l}{{\rm{m}}_{{{{\rm{(}}{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{10}}}}{{\rm{O}}_{\rm{5}}}{\rm{)}}}_{\rm{n}}}}} = {10^6} \times \frac{{75}}{{100}} = 75 \times {10^4}{\rm{ (g)}}\\ \Rightarrow {{\rm{n}}_{{{{\rm{(}}{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{10}}}}{{\rm{O}}_{\rm{5}}}{\rm{)}}}_{\rm{n}}}}} = \frac{{75 \times {{10}^4}}}{{162{\rm{n}}}}{\rm{ (mol)}}\\ \Rightarrow {{\rm{n}}_{{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{12}}}}{{\rm{O}}_{\rm{6}}}}} = {\rm{n}} \times {{\rm{n}}_{{{{\rm{(}}{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{10}}}}{{\rm{O}}_{\rm{5}}}{\rm{)}}}_{\rm{n}}}}} = {\rm{n}} \times \frac{{75 \times {{10}^4}}}{{162{\rm{n}}}} = \frac{{75 \times {{10}^4}}}{{162}}{\rm{ (mol)}}\\ \Rightarrow {{\rm{n}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = 2{{\rm{n}}_{{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{{\rm{12}}}}{{\rm{O}}_{\rm{6}}}}} = 2 \times \frac{{75 \times {{10}^4}}}{{162}} = \frac{{75 \times {{10}^4}}}{{81}}{\rm{ (mol)}}\\ \Rightarrow {{\rm{m}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = \frac{{75 \times {{10}^4}}}{{81}} \times 46 = \frac{{1150 \times {{10}^4}}}{{27}}{\rm{ (g)}}\\ \Rightarrow {{\rm{V}}_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = \frac{{1150 \times {{10}^4}}}{{27 \times 0.789}}{\rm{ (mL)}}\end{array}\)
Vì hiệu suất chung của cả quá trình điều chế ethanol là 70% và xăng E5 (chứa 5% ethanol về thể tích) nên
\({{\rm{V}}_{{\rm{E5}}}} = \frac{{1150 \times {{10}^4}}}{{27 \times 0.789}} \times \frac{{70}}{{100}} \times \frac{{100}}{5} \approx 7557620{\rm{ (mL) = 7557,62 (L)}}\)