Lý thuyết Tính chất hóa học của kim loại - Hóa 12 Cánh diều
Nhiều kim loại tác dụng được với các phi kim như oxygen, lưu huỳnh, halogen,…
I. Tác dụng với phi kim
Nhiều kim loại tác dụng được với các phi kim như oxygen, lưu huỳnh, halogen,…
Ví dụ: \(4{\rm{A}}l(s) + 3{O_2}(g) \to 2{\rm{A}}{l_2}{O_3}(s)\)
II. Tác dụng với nước
Trong môi trường trung tính, có:
2H 2 O + 2e \( \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} \)H 2 + OH - với E 2H2O/2OH-+H2 = -0,413V
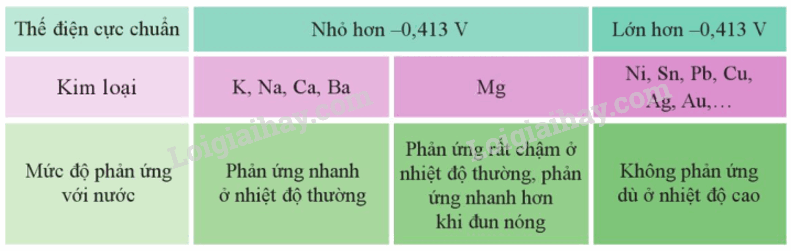
Cặp oxi hóa – khử M n+ /M có giá trị thế điện cực chuẩn nhỏ hơn – 0,413V thì kim loại M có thể tác dụng với nước ở nhiệt độ thường tạo thành hydroxide và khí hydrogen
III. Tác dụng với dung dịch muối
Kim loại không tan trong nước và có giá trị thế điện cực chuẩn nhỏ hơn thường tác dụng được với dung dịch muối của kim loại có giá trị thế điện cực lớn hơn ở điều kiện chuẩn.
Ví dụ: Zn(s) + CuSO 4 (aq) \( \to \) ZnSO 4 (aq) + Cu(s)
IV. Tác dụng với dung dịch acid
1. Tác dụng với dung dịch hydrochloric acid, dung dịch sulfuric acid loãng
Do \(E_{2{H^ + }/{H_2}}^o = 0V\)nên kim loại M có giá trị thế điện cực chuẩn \(E_{{M^{n + }}/M}^o < 0V\)có theẻ khử được ion H+ trong dung dịch hydrchloric acid hoặc dung dihcj sulfuric acid loãng, tạo thành khí H 2
Ví dụ: Zn(s) + 2H + (aq) \( \to \) Zn 2+ (aq) + H 2 (g)
Do giá trị thế điện cực chuẩn dương nên các kim loại như Cu, Ag,… không tác dụng với dung dịch hydrochloric acid hoặc dung dịch sulfuric acid loãng.
2. Tác dụng với dung dịch sulfuric acid đặc
Hầu hết các kim loại (trừ Au và Pt) phản ứng được với dung dịch sulfuric acid đặc. Phản ứng này thường tạo thành muối sulfate, nước và sulfur dioxide. Phản ứng diễn ra mạnh hơn khi hỗn hợp phản ứng được đun nóng
Ví dụ:
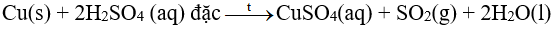
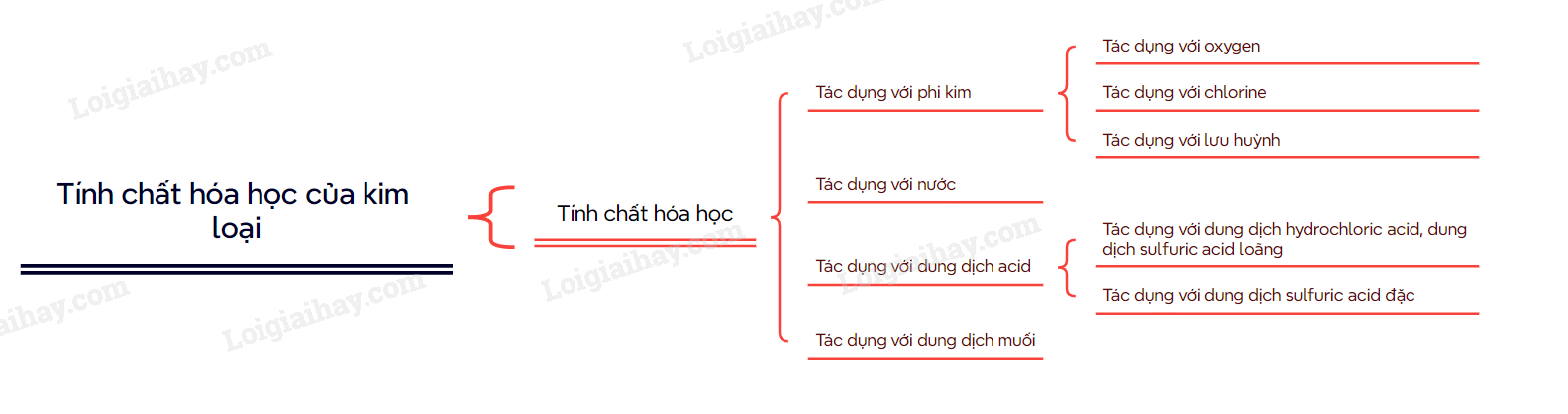
SƠ ĐỒ TƯ DUY