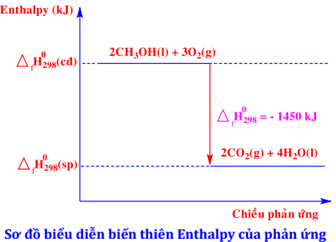
Phương trình nhiệt hoá học nào sau đây ứng với sơ đồ biểu diễn biến thiên enthalpy của phản ứng sau:
-
A.
\(2C{O_2}(g) + 4{H_2}O(l) \to 2C{H_3}OH(l) + 3{O_2}(g){\rm{ }}{\Delta _{\rm{r}}}{\rm{H}}_{298}^0 = 1450kJ\)
-
B.
\(2C{H_3}OH(l) + 3{O_2}(g) \to 2C{O_2}(g) + 4{H_2}O(l){\rm{ }}{\Delta _r}H_{298}^0 = 1450kJ\)
-
C.
\(2C{O_2}(g) + 4{H_2}O(l) \to 2C{H_3}OH(l) + 3{O_2}(g){\rm{ }}{\Delta _{\rm{r}}}{\rm{H}}_{298}^0 = - 1450kJ\)
-
D.
\(2C{H_3}OH(l) + 3{O_2}(g) \to 2C{O_2}(g) + 4{H_2}O(l){\rm{ }}{\Delta _r}H_{298}^0 = - 1450kJ\)
Dựa vào sơ đồ biểu diễn biến thiên enthalpy của phản ứng
\(2C{H_3}OH(l) + 3{O_2}(g) \to 2C{O_2}(g) + 4{H_2}O(l){\rm{ }}{\Delta _r}H_{298}^0 = - 1450kJ\)
Đáp án D
Đáp án : D