Đề bài
Quá trình hòa tan calcium chloride trong nước: \(CaC{l_2}(s) \to C{a^{2 + }}(aq) + 2C{l^ - }(aq)\)
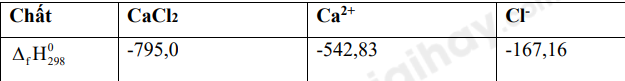
Biến thiên enthalpy của quá trình trên là:
-
A.
850,1 kJ
-
B.
850,1 kJ
-
C.
82,15 kJ
-
D.
-82,15 kJ
Phương pháp giải
Dựa vào enthalpy tạo thành chuẩn của các chất
\({\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0(C{a^{2 + }}) + 2.{\Delta _f}H_{298}^0(C{l^ - }) - {\Delta _f}H_{298}^0(CaC{l_2})\)
= -542,83 + 2.-167,16 – (-795,0) = -82,15 KJ
Đáp án D
Đáp án : D