Ôn tập chương 1 trang 17, 18 SBT Hóa 10 Chân trời sáng tạo
Nguyên tử là phần tử nhỏ nhất của chất và A. không mang điện. B. mang điện tích dương. C. mang điện tích âm. D. có thể mang điện hoặc không mang đến Phát biểu nào sau đây không đúng? A. Chỉ có hạt nhân nguyên tử oxygen mới có 8 proton. B. Chỉ có hạt nhân nguyên tử oxygen mới có 8 neutron. C. Chỉ có nguyên tử oxygen mới có 8 electron. D. Cả A và C.
1.1
Nguyên tử là phần tử nhỏ nhất của chất và
A. không mang điện.
B. mang điện tích dương.
C. mang điện tích âm.
D. có thể mang điện hoặc không mang đến
Phương pháp giải:
Dựa vào đặc điểm của nguyên tử: Nguyên tử có kích thước vô cùng nhỏ và trung hòa về điện
Lời giải chi tiết:
- Đáp án: A
1.2
Phát biểu nào sau đây không đúng?
A. Chỉ có hạt nhân nguyên tử oxygen mới có 8 proton.
B. Chỉ có hạt nhân nguyên tử oxygen mới có 8 neutron.
C. Chỉ có nguyên tử oxygen mới có 8 electron.
D. Cả A và C.
Phương pháp giải:
Dựa vào
- Đặc điểm: hạt nhân mỗi nguyên tử chỉ chứa số lượng proton đặc trưng cho nguyên tử của nguyên tố đó
- Số p = số e
Lời giải chi tiết:
- Đáp án: B
1.3
Số hiệu nguyên tử cho biết
A. số proton trong hạt nhân nguyên tử hoặc số đơn vị điện tích hạt nhân nguyên tử.
B. số electron trong lớp vỏ nguyên tử.
C. số thứ tự của nguyên tố trong bảng tuần hoàn.
D. cả A, B và C đều đúng.
Phương pháp giải:
Dựa vào ý nghĩa của số hiệu nguyên tử: Số hiệu nguyên tử cho biết:
- Số proton trong hạt nhân nguyên tử hoặc số đơn vị điện tích hạt nhân nguyên tử.
- Số electron trong lớp vỏ nguyên tử.
- Số thứ tự của nguyên tố trong bảng tuần hoàn.
Lời giải chi tiết:
- Đáp án: D
1.4
Cấu hình electron nào sau đây là của nguyên tử fluorine (Z = 9)?
A 1s 2 2s 2 2p 3
B. 1s 2 2s 2 2p 4
C. 1s 2 2s 3 2p 4
D. 1s 2 2s 2 2p 5
Phương pháp giải:
Viết cấu hình electron của nguyên tử
- Bước 1: Xác định số electron của nguyên tử
- Bước 2: Các electron được phân bố theo thứ tự các AO có mức năng lượng tăng dần, theo các nguyên lí và quy tắc phân bố electron trong phân tử
- Bước 3: Viết cấu hình electron theo thứ tự các phân lớp trong một lớp và theo thứ tự của các lớp electron
Lời giải chi tiết:
- Nguyên tử F có 9 electron
=> Phân mức năng lượng electron: 1s 2 2s 2 2p 5
=> Cấu hình electron của nguyên tử F: 1s 2 2s 2 2p 5
=> Đáp án: D
1.5
Nguyên tử của nguyên tố phosphorus (Z = 15) có số electron độc thân là
A.1
B. 2.
C. 3.
D. 4.
Phương pháp giải:
Viết cấu hình electron của nguyên tử
- Bước 1: Xác định số electron của nguyên tử
- Bước 2: Các electron được phân bố theo thứ tự các AO có mức năng lượng tăng dần, theo các nguyên lí và quy tắc phân bố electron trong phân tử
- Bước 3: Viết cấu hình electron theo thứ tự các phân lớp trong một lớp và theo thứ tự của các lớp electron
=> Viết cấu hình electron theo ô lượng tử của nguyên tử
=> Xác định số electron độc thân
Lời giải chi tiết:
- Nguyên tử P có 15 electron
=> Phân mức năng lượng electron: 1s 2 2s 2 2p 6 3s 2 3p 3
=> Cấu hình electron của nguyên tử P: 1s 2 2s 2 2p 6 3s 2 3p 3
=> Cấu hình electron theo ô lượng tử của nguyên tử P:
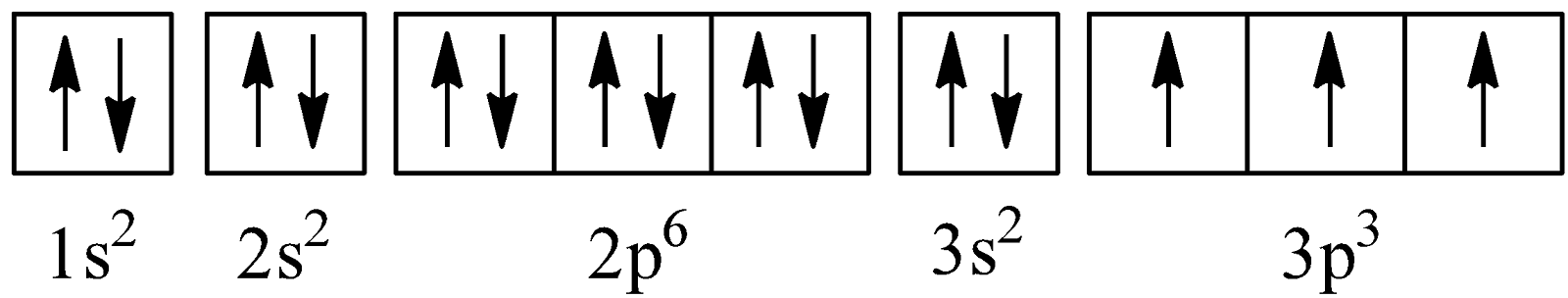
=> Nguyên tử P có 3 electron độc thân
1.6
Trong từ nhiên, bromine có 2 đồng vị \({}_{35}^{79}Br\) có hàm lượng 50,7% và \({}_{35}^{81}Br\) có hàm lượng 49,3%. Tính nguyên tử khối trung bình của bromine.
Phương pháp giải:
Dựa vào công thức tính nguyên tử khối trung bình của nguyên tố X:
\(\overline A {}_X = \frac{{{a_1}.A{}_1 + {a_2}.{A_2} + ... + {a_i}.{A_i}}}{{100}}\)
Trong đó:
- \(\overline A {}_X\)là nguyên tử khối trung bình của X
- A i là nguyên tử khối đồng vị thứ i
- a i là tỉ lệ % số nguyên tử đồng vị thứ i
Lời giải chi tiết:
- Nguyên tử khối trung bình của bromine là
\(\overline M {}_{Br} = \frac{{50,7.79 + 49,3.81}}{{100}}\)= 79,986 (g/mol)
1.7
Lithium trong tự nhiên có 2 đồng vị là \({}_3^7Li\) và \({}_3^6Li\). Nguyên tử khối trung bình của lithium là 6,94. Tinh thành phần phần trăm của mỗi đồng vị lithium trong tự nhiên.
Phương pháp giải:
Dựa vào công thức tính nguyên tử khối trung bình của nguyên tố X:
\(\overline A {}_X = \frac{{{a_1}.A{}_1 + {a_2}.{A_2} + ... + {a_i}.{A_i}}}{{100}}\)
Trong đó:
- \(\overline A {}_X\)là nguyên tử khối trung bình của X
- A i là nguyên tử khối đồng vị thứ i
- a i là tỉ lệ % số nguyên tử đồng vị thứ i
Lời giải chi tiết:
- Gọi thành phần phần trăm của đồng vị \({}_3^7Li\) là x (%)
=> Thành phần phần trăm của đồng vị \({}_3^6Li\) là 100-x (%)
- Áp dụng công thức tính nguyên tử khối trung bình ta có:
\(\overline M {}_{Li} = \frac{{x.7 + (100 - x).6}}{{100}}\)= 6,94 " x = 94%
=> Vậy thành phần phần trăm của đồng vị \({}_3^7Li\) là 94% và thành phần phần trăm của đồng vị \({}_3^6Li\) là 100 - 94 = 6%
1.8
Điện tích của electron là -1,602.10 -19 C (coulomb). Tính điện tích của hạt nhân nguyên tử carbon theo đơn vị coulomb.
Phương pháp giải:
Dựa vào
- Điện tích của electron là -1,602.10 -19 C (coulomb)
- Điện tích hạt nhân = số proton = số electron
- Điện tích hạt nhân (tính theo coulomb) = số proton x 1,602.10 -19 C
Lời giải chi tiết:
- Nguyên tử carbon có Z = 6
=> Điện tích hạt nhân (tính theo coulomb) = 6 x 1,602.10 -19 C = 9,612.10 -19 C
1.9
Hợp chất Y có công thức MX 2 (là hợp chất được sử dụng làm cơ chế đánh lửa bằng bánh xe trong các dạng súng cổ), trong đó M chiếm 46,67% về khối lượng. Trong hạt nhân M có số neutron nhiều hơn số proton là 4 hạt. Trong hạt nhân nguyên tử X, số neutron bằng số proton. Tổng số proton trong MX 2 là 58.
a) Tìm A M và A X
b) Xác định công thức phân tử của MX 2
Phương pháp giải:
Dựa vào
- Mối liên hệ giữa các hạt proton (p), neutron (n) và electron (e) trong nguyên tử:
+ Số neutron nhiều hơn số proton là X hạt " n - p = X
+ Trong nguyên tử trung hòa về điện có p = e
+ Số khối A = p + n
- Công thức tính phần trăm khối lượng của nguyên tố X trong hợp chất X a Y b :
\(\% {A_X} = \frac{{a.{A_X}}}{{{M_{{X_a}{Y_b}}}}}.100\% = \frac{{a.{A_X}}}{{a.{A_X} + b.{A_Y}}}.100\% \)
Lời giải chi tiết:
a) - Gọi số hạt proton, electron và neutron trong nguyên tử M lần lượt là p 1 , e 1 , n 1
- Gọi số hạt proton, electron và neutron trong nguyên tử X lần lượt là p 2 , e 2 , n 2
- Trong hạt nhân M có số neutron nhiều hơn số proton là 4 hạt " n 1 - p 1 = 4 (1)
- Trong hạt nhân nguyên tử X, số neutron bằng số proton " n 2 = p 2 (2)
- Tổng số proton trong MX 2 là 58 " p 1 + 2.p 2 = 58 (3)
- Nguyên tử M chiếm 46,67% về khối lượng
=> \(\% {A_M} = \frac{{1.{A_M}}}{{1.{A_M} + 2.{A_X}}}.100\% = \frac{{{p_1} + {n_1}}}{{{p_1} + {n_1} + 2.({p_2} + {n_2})}}.100\% \) = 46,67% (4)
=> Từ (1), (2), (3), (4) giải hệ 4 phương trình 4 ẩn ta có: p 1 = 26, n 1 = 30,
p 2 = n 2 = 16
=> Vậy A M = 26 + 30 = 56, A X = 16 + 16 = 32
b) Công thức phân tử của MX 2 là FeS 2
1.10
Hợp chất có công thức phân tử M 2 X (được ứng dụng trong sản xuất xi măng, phần bón) có tổng số hạt là 140. Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 44. Số khối của nguyên tử M lớn hơn số khối của nguyên tử X là 23. Tổng số hạt trong nguyên tử M nhiều hơn trong nguyên tử X là 34. Viết cấu hình electron của các nguyên tử M và X. Viết công thức phân tử của hợp chất M 2 X
Phương pháp giải:
Dựa vào mối liên hệ giữa các hạt proton (p), neutron (n) và electron (e) trong nguyên tử:
- Tổng số hạt trong nguyên tử = p + n + e
- Trong nguyên tử trung hòa về điện có p = e
- Số hạt không mang điện = n
- Proton mang điện tích dương, electron mang điện tích âm
- Số khối A = p + n
*Viết cấu hình electron của nguyên tử
- Bước 1: Xác định số electron của nguyên tử
- Bước 2: Các electron được phân bố theo thứ tự các AO có mức năng lượng tăng dần, theo các nguyên lí và quy tắc phân bố electron trong phân tử
- Bước 3: Viết cấu hình electron theo thứ tự các phân lớp trong một lớp và theo thứ tự của các lớp electron
Lời giải chi tiết:
- Gọi số hạt proton, electron và neutron trong nguyên tử M lần lượt là p 1 , e 1 , n 1
- Gọi số hạt proton, electron và neutron trong nguyên tử X lần lượt là p 2 , e 2 , n 2
- Có tổng số hạt là 140 " 2.(p 1 + e 1 + n 1 ) + p 2 + e 2 + n 2 = 140 (1)
- Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 44
=> (2.(p 1 + e 1 ) + p 2 + e 2 ) - (2.n 1 + n 2 ) = 44 (2)
- Số khối của nguyên tử M lớn hơn số khối của nguyên tử X là 23
=> (p 1 + n 1 ) - (p 2 + n 2 ) = 23 (3)
- Tổng số hạt trong nguyên tử M nhiều hơn trong nguyên tử X là 34
=> (p 1 + e 1 + n 1 ) - (p 2 + e 2 + n 2 )= 34 (4)
=> Từ (1), (4) giải hệ hai phương trình hai ẩn (p 1 + e 1 + n 1 ) và (p 2 + e 2 + n 2 )ta có
(p 1 + e 1 + n 1 ) = 58 (5) và (p 2 + e 2 + n 2 ) = 24 (6)
- Có p 1 = e 1 và p 2 = e 2 thay vào các phương trình (2), (5), (6) ta được
(2’) (2.2p 1 + 2p 2 ) - (2.n 1 + n 2 ) = 44
(5’) 2p 1 + n 1 = 58
(6’) 2p 2 + n 2 = 24
=> Từ (2’), (3), (5’), (6’) giải hệ bốn phương trình bốn ẩn ta có p 1 = e 1 = 19,
n 1 = 20, p 2 = e 2 = 8, n 2 = 8
- Nguyên tử M có 19 electron " M là nguyên tố Potassium (K)
=> Phân mức năng lượng electron: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1
=> Cấu hình electron của nguyên tử M: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1
- Nguyên tử X có 8 electron " X là nguyên tố Oxygen (O)
=> Phân mức năng lượng electron: 1s 2 2s 2 2p 4
=> Cấu hình electron của nguyên tử X: 1s 2 2s 2 2p 4
=> Vậy công thức phân tử của hợp chất M 2 X là K 2 O