Bài 15. Tách kim loại và tái chế kim loại trang 49, 50 SBT Hóa 12 Cánh diều
Trong vỏ Trái Đất, những kim loại nào sau đây tồn tại chủ yếu dưới dạng đơn chất.
15.1
Trong vỏ Trái Đất, những kim loại nào sau đây tồn tại chủ yếu dưới dạng đơn chất.
A. Ag, Au. B. Zn, Fe. C. Mg, Al. D. Na, Ba.
Phương pháp giải:
Dựa vào trạng thái tự nhiên của kim loại.
Lời giải chi tiết:
Ag, Au tồn tại chủ yếu ở dạng đơn chất vì Ag, Au gần như trơ về mặt hóa học ở điều kiện thường.
Đáp án A
15.2
Trong tự nhiên, nguyên tố kim loại có thể được tìm thấy ở đâu?
(1) Nước ngầm. (2) Nước biển.
(3) Đất đá. (4) Cây xanh có hoa.
A. (1), (2) và (3). B. (2) và (3).
C. (1) và (3). D. (1), (2), (3) và (4).
Phương pháp giải:
Dựa vào trạng thái tự nhiên của kim loại.
Lời giải chi tiết:
Trong tự nhiên, nguyên tố kim loại có thể tìm thấy ở nước ngầm, nước biển, đất đá.
Đáp án A
15.3
Nguyên tắc tách kim loại ra khỏi hợp chất của chúng là
A. Khử ion kim loại trong hợp chất thành nguyên tử.
B. Oxy hoá ion kim loại trong hợp chất thành nguyên tử.
C. Hoà tan các khoàng vật có trong quặng để thu được kim loại.
D. Dựa trên tính chất của kim loại như từ tính , khối lượng riêng lớn để tách chúng ra khỏi quặng.
Phương pháp giải:
Dựa vào nguyên tắc tách kim loại.
Lời giải chi tiết:
Khử ion kim loại trong hợp chất thành nguyên tử.
Đáp án A
15.4
Với quá trình tách natri (sodium) bằng phương pháp điện phân sodium chloride nóng chảy, phát biểu nào sau đây đúng?
A. Tại anode xảy ra quá trình khử ion Na + .
B. Tại cathode xảy ra quá trình khử ion Cl - .
C. Tại cathode xảy ra quá trình khử ion Na + .
D. Tại anode xảy ra quá trình khử ion Cl - .
Phương pháp giải:
Dựa vào nguyên tắc phương pháp điện phân.
Lời giải chi tiết:
Khi điện phân nóng chảy NaCl, tạo cathode xảy ra quá trình khử ion Na + : Na + + 1e \( \to \)Na.
Đáp án C
15.5
Cho các kim loại Ag, Al, Cu, Fe, Mg, Na, Sn, Zn. Tìm hiểu và sắp xếp các kim loại trên vào ô tương ứng với phương pháp phù hợp để tách chúng ra khỏi hợp chất.
|
Phương pháp |
Kim loại |
|
Nhiệt luyện |
|
|
Thuỷ luyện |
|
|
Điện phân nóng chảy |
Phương pháp giải:
Dựa vào các phương pháp tách kim loại.
Lời giải chi tiết:
|
Phương pháp |
Kim loại |
|
Nhiệt luyện |
Cu, Fe, Sn, Zn… |
|
Thuỷ luyện |
Ag, Cu, Fe, Sn, Zn |
|
Điện phân nóng chảy |
Al, Mg, Na |
15.6
Trong phản ứng tách kim loại từ ZnO bằng C theo phương pháp nhiệt luyện, kẽm sinh ra ở thể nào? Vì sao?
Phương pháp giải:
Dựa vào phương pháp tách kim loại.
Lời giải chi tiết:
Kẽm sinh ra trong quá trình nhiệt luyện ở thể hơi, vì phản ứng nhiệt luyện có nhiệt độ cao, kẽm có nhiệt độ nóng chảy thấp.
15.7
Chu sa còn gọi là cinnabar, là một loại khoáng vật có thành phần chính là HgS. Trước đây trong y học cổ truyền, chu sa được dùng với liều lượng phù hợp kết hợp với một số vị thuốc khác trong điều trị chứng mất ngủ, tim đập loạn, hồi hộp. Tuy nhiên, vị thuốc này chỉ được “ dùng sống ” , thuyệt đối KHÔNG nấu (không sắc thuốc), hoặc dùng lửa (nướng, đốt) [1] . Hãy tìm hiểu và lí giải cho việc không dùng nhiệt đối với chu sa, Viết phương trình hóa học của phản ứng xảy ra (nếu có).
Phương pháp giải:
Dựa vào tính chất hóa học của kim loại.
Lời giải chi tiết:
Muối HgS dễ bị phân hủy, cháy khi đun nóng hoặc tiếp xúc với lửa, sinh ra hơi thủy ngân rất độc. Trong thực tế, trước đây người ta dùng đá chu sa như một nguồn chủ yếu để sản xuất kim loại thủy ngân, người ta đốt cháy chu sa trong ống kín, ngưng tụ sản phẩm cháy thu được thủy ngân ở dạng lỏng.
HgS(s) → Hg(g) + S(s)
HgS(s) + O 2 (g) → Hg(g) + SO 2 (g)
15.8
Trong công nghiệp, nhôm được điều chế bằng cách điện phân nóng chảy hỗn hợp alumina (Al 2 O 3 ) và cryolite (Na 3 AlF 6 ) còn gọi là quy trình Hall-Héroul: 2Al 2 O 3 ( l ) 4Al( l ) + 3O 2 (g) như hình dưới đây. Nhiệt độ nóng chảy của hỗn hợp alumina và cryolite khoảng 950 o C, thấp hơn nhiều so với nhiệt độ nóng chảy của alumina (> 2000 o C); ngoài ra, cryolite còn làm tăng độ dẫn điện của hỗn hợp nóng chảy. trong quá trình điện phân, cực dương làm bằng graphite bị ăn mòn và liên tục bị nhúng xuống bể điện phân. Sau một thời gian, các thanh graphite này sẽ được thay mới.
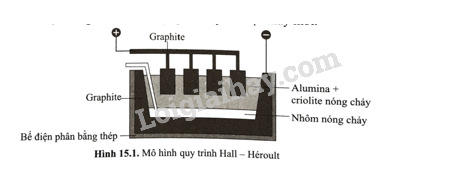
Mỗi phát biểu sau đây là đúng hay sai?
A. Nhôm kim loại được tách ra tại cathode.
B. Cryolite được thêm vào bể điện phân giúp tiết kiệm được năng lượng, giảm chi phí sản xuất.
C. Bên cạnh nhôm, oxygen tinh khiết cũng thu được trực tiếp từ quy trình này.
D. Vì anode và cathode đều làm bằng graphite, nên nếu đổi chiều dòng điện (anode trở thành cathode và ngược lại) thì quy trình điện phân vẫn xảy ra bình thường.
Phương pháp giải:
Dựa vào phương pháp điện phân nóng chảy.
Lời giải chi tiết:
a. Đúng. Tại cathode (-): Al 3+ (l) + 3e → Al(l), theo hình vẽ, lớp nhôm nóng chảy thu được tại cực âm (phần đáy của bể điện phân).
b. Đúng. Cryolite làm giảm sâu nhiệt độ nóng chảy, từ đó giảm lượng năng lượng cần cung cấp để nấu chảy hỗn hợp. Ngoài ra, việc tăng độ dẫn điện còn làm tăng hiệu suất của quá trình điện phân. Do đó, làm giảm chi phí sản xuất.
c. Sai. Tại anode, graphite bị ăn mòn do phản ứng với oxygen tạo thành các oxide của carbon thoát ra cùng với oxygen.
C(s) + O 2 (g) → CO 2 (g)
C(s) + CO 2 (g) → 2CO(g)
d. Sai. Việc thiết kế cathode bên dưới bể điện phân giúp nhôm nóng chảy sinh ra ở đáy bể tráng tiếp xúc với oxygen trong không khí, ngoài ra tỉ trọng của nhôm lỏng lớn hơn hỗn hợp điện phân giúp nhôm lỏng chìm xuống đáy bể, không ảnh hưởng đến quá trình điện phân. Anode ở phía trên dễ dàng nhúng xuống bể liên tục khi bị ăn mòn (việc này gần như không thể thực hiện nếu đặt anode ở đáy bể). Bên cạnh đó, nếu anode ở đáy bể, các khi sinh ra tại anode sẽ thoát vào hỗn hợp lỏng, ảnh hưởng đến quá trình điện phân.