Bài 7. Tốc độ phản ứng và chất xúc tác trang 23, 24, 25 SBT Khoa học tự nhiên 8 - Kết nối tri thức
Than cháy trong bình khí oxygen nhanh hơn cháy trong không khí. Yếu tố đã làm tăng tốc độ của phản ứng này là
7.1
Than cháy trong bình khí oxygen nhanh hơn cháy trong không khí. Yếu tố đã làm tăng tốc độ của phản ứng này là
A. tăng nhiệt độ. B. tăng nồng độ.
C. tăng diện tích bề mặt tiếp xúc. D. dùng chất xúc tác.
Phương pháp giải:
Dựa vào các yếu tố làm tăng tốc độ phản ứng
Lời giải chi tiết:
Nồng độ khí oxygen trong không khí là nhỏ hơn nồng độ oxygen trong bình chứa oxygen.
Đáp án: B
7.2
Để điều chế CO 2 trong phòng thí nghiệm, người ta cho đá vôi (rắn) phản ứng với dung dịch hydrochloric acid. Phản ứng xảy ra như sau:
CaCO 3 + 2HCl → CaCl 2 + H 2 O + CO 2 .
Biện pháp nào sau đây không làm phản ứng xảy ra nhanh hơn?
A. Đập nhỏ đá vôi. B. Tăng nhiệt độ phản ứng.
C. Thêm CaCl 2 vào dung dịch. D. Dùng HCl nồng độ cao hơn.
Phương pháp giải:
Dựa vào các yếu tố làm tăng tốc độ phản ứng
Lời giải chi tiết:
Đập nhỏ đá vôi → tăng diện tích tiếp xúc → tăng tốc độ phản ứng.
Tăng nhiệt độ phản ứng → tăng tốc độ phản ứng.
Dùng HCl nồng độ cao hơn → tăng nồng độ chất tham gia → tăng tốc độ phản ứng.
Đáp án: C
7.3
Trong các câu sau, câu nào đúng, câu nào sai?
a) Phản ứng giữa nước chanh và nước rau muống (xuất hiện màu hồng nhạt) là phản ứng hoá học xảy ra nhanh.
b) Phản ứng lên men rượu xảy ra chậm.
c) Phản ứng cháy nổ xảy ra chậm.
d) Phản ứng đốt cháy than trong không khí nhanh hơn phản ứng sắt bị gỉ trong không khí.
Phương pháp giải:
Dựa vào các yếu tố làm tăng tốc độ phản ứng
Lời giải chi tiết:
(a); (b); (d) đúng.
(c) sai vì phản ứng nổ diễn ra với tốc độ rất nhanh.
7.4
Có hai thanh kim loại nikel cùng khối lượng. Một thanh có nhiều lỗ rỗng trên bề mặt, thanh kia có bề mặt mịn và chắc. Ngâm hai thanh vào cốc đựng dung dịch HCl. Phản ứng xảy ra như sau: Ni + 2HCl → NiCl 2 + H 2 .
Sau một thời gian phản ứng, lấy hai thanh kim loại ra cân, thu được kết quả như sau:
- Thanh kim loại thứ nhất: khối lượng giảm 0,15 g.
- Thanh kim loại thứ hai: khối lượng giảm 0,21 g.
Hãy cho biết thanh kim loại nikel nào có diện tích bề mặt tiếp xúc với acid lớn hơn.
Phương pháp giải:
Tốc độ phản ứng và chất xúc tác
Lời giải chi tiết:
Phản ứng ở thanh thứ hai nhanh hơn (do khối lượng giảm nhiều hơn trong cùng một đơn vị thời gian). Vậy thanh thứ hai có nhiều lỗ rỗng li ti trên bề mặt do diện tích tiếp xúc lớn hơn.
7.5
Cho hai miếng kẽm giống nhau vào hai ống nghiệm đựng dung dịch H 2 SO 4 cùng nồng độ. Một ống để ở nhiệt độ phòng, một ống ngâm trong cốc nước nóng. Phản ứng xảy ra như sau:
Zn + H 2 SO 4 → ZnSO 4 + H 2 .
Đo thể tích khí thoát ra tại mỗi ống nghiệm sau 30 giây, thu được kết quả như sau:
- Ống nghiệm 1: thu được 5 mL khí.
- Ống nghiệm 2: thu được 7 mL khí.
Hãy cho biết ống nghiệm nào được đặt trong cốc nước nóng. Giải thích.
Phương pháp giải:
Dựa vào thể tích khí thu được ở 2 ống nghiệm
Lời giải chi tiết:
Phản ứng ở ống nghiệm 2 xảy ra nhanh hơn (vì thể tích khí thoát ra trong cùng một đơn vị thời gian nhiều hơn). Vậy ống nghiệm 2 được đặt trong nước nóng.
7.6
Thực hiện thí nghiệm sau:
Lấy hai ống nghiệm giống hệt nhau, kí hiệu lần lượt là A và B.
Cho vào 2 ống nghiệm cùng một khối lượng dung dịch HCl nhưng nồng độ các dung dịch khác nhau.
Cho cùng một lượng đá vôi dạng viên vào 2 ống nghiệm trên. Phản ứng xảy ra như sau:
CaCO 3 + 2HCl → CaCl 2 + H 2 O + CO 2
Sau 1 phút, cân lại khối lượng hai ống nghiệm. Thu được kết quả sau:
- Ống nghiệm A: khối lượng giảm 0,44 g.
- Ống nghiệm B: khối lượng giảm 0,56 g.
Hãy cho biết dung dịch trong ống nghiệm nào có nồng độ cao hơn. Giải thích.
Phương pháp giải:
Dựa vào khối lượng giảm ở hai ống nghiệm A, B
Lời giải chi tiết:
Khí CO 2 thoát ra làm khối lượng hỗn hợp giảm.
Trong cùng một khoảng thời gian, khối lượng ống nghiệm B giảm nhiều hơn nên phản ứng xảy ra trong B nhanh hơn. Vậy dung dịch trong ống nghiệm B có nồng độ cao hơn.
7.7
7 Phản ứng phân huỷ H 2 O 2 xảy ra như sau: 2H 2 O 2 → 2H 2 O + O 2 .
Người ta cho 5 mL dung dịch H 2 O 2 (cùng nồng độ) vào 5 ống nghiệm. Sau đó lần lượt cho vào 4 ống nghiệm lượng nhỏ các chất Fe, MnO 2 , KI, SiO 2 và một ống giữ nguyên. Đun nóng 5 ống nghiệm ở cùng một nhiệt độ và đo thời gian đến khi phản ứng kết thúc. Kết quả thu được được trình bày trên biểu đồ như sau:
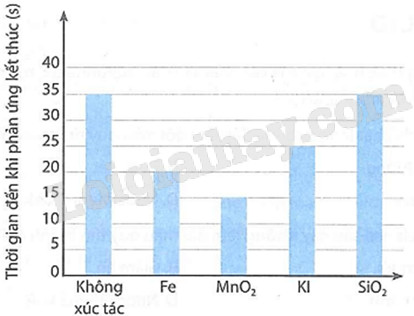
Từ biểu đồ trên hãy cho biết:
a) chất nào có tác dụng xúc tác tốt nhất (làm phản ứng xảy ra nhanh nhất).
b) chất nào không có tác dụng xúc tác.
Phương pháp giải:
Tốc độ phản ứng và chất xúc tác
Lời giải chi tiết:
a) MnO 2 có khả năng xúc tác tốt nhất (làm phản ứng xảy ra nhanh nhất).
b) SiO 2 không có tác dụng xúc tác (vì không làm thay đổi tốc độ phản ứng).
7.8
Một bạn học sinh thực hiện thí nghiệm như sau: Lấy một ít cơm nguội để trong một cái bát (chén) và bọc kín. Một bát để trong tủ lạnh (khoảng 5 °C), một bát để ở nhiệt độ phòng (khoảng 35 °C). Bạn đó theo dõi thấy cơm ở nhiệt độ phòng bắt đẩu thiu sau 12 giờ, trong khi đó cơm ở tủ lạnh bắt đầu thiu sau 84 giờ (3,5 ngày). Tốc độ phản ứng cơm bị oxi hoá (cơm thiu) ở nhiệt độ phòng lớn hơn ở nhiệt độ tủ lạnh bao nhiêu lần?
Phương pháp giải:
Dựa vào tốc độ phản ứng cơm bị thiu ở hai nhiệt độ khác nhau
Lời giải chi tiết:
Tốc độ phản ứng tỉ lệ nghịch với thời gian.
Vậy tốc độ phản ứng oxi hoá cơm ở nhiệt độ phòng lớn hơn ở nhiệt độ tủ lạnh: \(\frac{{84}}{{12}}\)= 7 lần.