Lý thuyết Amine - Hóa 12 Cánh diều
Khi thay thế một hay nhiều nguyên tử hydrogen trong phân tử ammonia bằng một hay nhiều gốc hydrocarbon thu được amine.
I. Khái niệm, phân loại và danh pháp
Khi thay thế một hay nhiều nguyên tử hydrogen trong phân tử ammonia bằng một hay nhiều gốc hydrocarbon thu được amine.
2. Phân loại
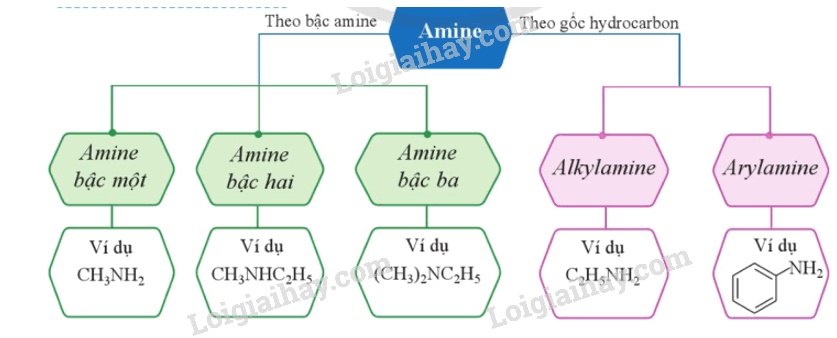
3. Danh pháp
Theo danh pháp gốc – chức, tên của amine được hình thành từ tên của các gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen kèm theo tên chức amine
Theo danh pháp thay thế, các amine đơn chức được gọi tên như sau:
+ Amine bậc một: tên hydrocarbon (bỏ e) + vị trí nhóm –NH2 + amine
+ Amine bậc hai: N – tên gốc hydrocarbon + tên hydrocarbon mạch dài nhất (bỏ e) + vị trí nhóm chức amine + amine
+ Amine bậc ba: N – tên gốc hydrocarbon thứ nhất + N – tên gốc hydrocarbon thứ hai + tên hydrocarbon mạch dài nhất (bỏ e) + vị trí nhóm chức amine + amine.
II. Tính chất vật lý
- Methylamine, dimethylamine, trimethylamine và ethylamine là những chất khí ở điều kiện thường. Các amine có phân tử phối lớn hơn là chất lỏng hoặc chất rắn.
- Các amine có khối lượng phân tử thấp thường có mùi khó chịu
- Amine thường có nhiệt độ sôi cao hơn so với nhiệt độ sôi của các hydrocarbon có cùng số nguyên tử carbon hoặc có phân tử khối gần với chúng
III. Tính chất hóa học
1. Tính base và phản ứng tạo phức
- Dung dịch aniline trong nước không làm đổi màu quỳ tím, trong khi dung dịch các alkylamine có thể làm quỳ tím hóa xanh. Amine tác dụng với acid tạo thành muối. Các amine có khối lượng phân tử nhỏ có khả năng tác dụng với dung dịch muoói của một số kim loại tạo thành kết tủa hydroxide.
Ví dụ: C 2 H 5 NH 2 + HCl \( \to \)[C 2 H 5 NH 3 ] + Cl -
3C 2 H 5 NH 2 + FeCl 3 + 3H 2 O\( \to \)Fe(OH) 3 + 3[C 2 H 5 NH 3 ] + Cl -
2. Tính khử
Alkylamine bậc một tác dụng với nitrous acid ở nhiệt độ thường tạo thành alcohol và giải phóng nitrogen
Ví dụ: C 2 H 5 NH 2 + HONO \( \to \) C 2 H 5 OH + N 2 + H 2 O
3. Phản ứng thế ở nhân thơm của aniline
Nhóm – NH 2 trong phân tử aniline làm tăng mật độ electron trong vòng benzene, đặc biệt ở các vị trí ortho và para. Aniline dễ tham gia phản ứng với nước bromine tạo 2,4,6 – tribromoaniline kết tủa trắng.
IV. Ứng dụng và điều chế
1. Ứng dụng
- Hợp chất có nhóm chức amine được thấy trong thành phần của nhiều dược phẩm, thuốc bảo vệ thực vật,…
- Aniline là nguyên liệu quan trọng để tổng hợp phẩm nhuộm, chất hoạt động bề mặt.
2. Điều chế
a) Alkyl hóa ammonia
alkylamine được điều chế từ ammonia và dẫn xuất halogen.
Ví dụ:
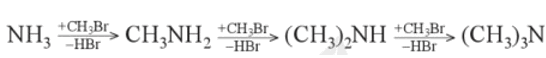
b) Khử hợp chất nitro
Arylamine thường được điều chế bằng cách khử dẫn xuất nitro tương ứng. Tác nhân khử thường dùng là kim loại trong hydrochloric acid
Ví dụ:

SƠ ĐỒ TƯ DUY
