Bài 15. Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng trang 94, 95, 96, 97 Hóa 10 Chân trời sáng tạo
Trong tự nhiên có những phản ứng xảy ra rất nhanh, như phản ứng nổ của pháo hoa, phản ứng cháy của que diêm,… 1. Quan sát hình trong phần Khởi động, nhận xét về mức độ nhanh hay chậm của phản ứng hóa học xảy ra trong đám cháy lá cây khô và thân tàu biển bị oxi hóa trong điều kiện tự nhiên
CH tr 94 MĐ
|
Trong tự nhiên có những phản ứng xảy ra rất nhanh, như phản ứng nổ của pháo hoa, phản ứng cháy của que diêm,… nhưng cũng có những phản ứng xảy ra chậm hơn, như quá trình oxi hóa các kim loại sắt, đồng trong khí quyển, sự ăn mòn vỏ tàu biển làm bằng thép,… Để đánh giá mức độ nhanh hay chậm của một phản ứng hóa học cần dùng đại lượng nào? Cách tính ra sao?
|
Lời giải chi tiết:
- Để đánh giá mức độ nhanh hay chậm của một phản ứng hóa học, người ta dùng đại lượng: tốc độ phản ứng
- Cách tính: Cho phản ứng tổng quát:
aA + bB → cC + dD
Biểu thức tốc độ trung bình của phản ứng:
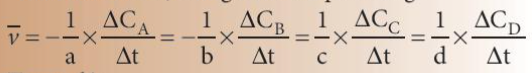
Trong đó:
\(\mathop v\limits^\_ \): tốc độ trung bình của phản ứng
∆C = C 2 – C 1 : sự biến thiên nồng độ
∆t = t 2 – t 1 : biến thiên thời gian
C 1 , C 2 là nồng độ của một chất tại 2 thời điểm tương ứng t 1 , t 2
CH tr 94 CH
|
1 . Quan sát hình trong phần Khởi động, nhận xét về mức độ nhanh hay chậm của phản ứng hóa học xảy ra trong đám cháy lá cây khô và thân tàu biển bị oxi hóa trong điều kiện tự nhiên
|
Lời giải chi tiết:
- Trong đám cháy của lá cây khô: Phản ứng hóa học xảy ra nhanh. Các lá cây nhanh chóng bị cháy và chuyển thành tro
- Thân tàu biển bị oxi hóa trong điều kiện tự nhiên: Phản ứng hóa học xảy ra chậm. Vỏ tàu biển làm bằng thép mất thời gian rất lâu mới bị gỉ (bị oxi hóa)
CH tr 95 CH
|
2. Trong tự nhiên và cuộc sống, ở cùng điều kiện, nhiều chất khác nhau sẽ biến đổi hóa học nhanh, chậm khác nhau; với cùng một chất, trong điều kiện khác nhau cũng biến đổi hóa học nhanh, chậm khác nhau. Tìm các ví dụ minh họa cho 2 nhận định trên |
Phương pháp giải:
- Ví dụ: Đốt cháy
CH tr 95 CH
|
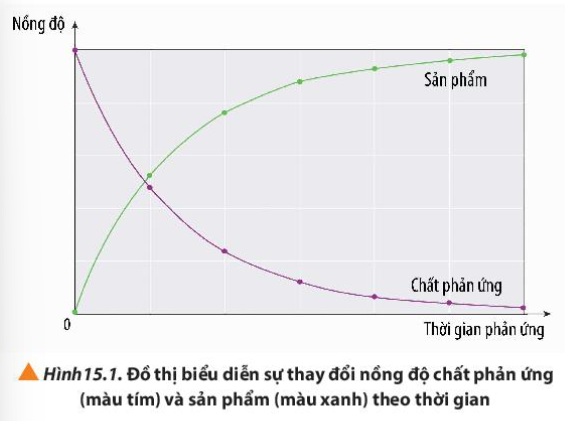
3. Quan sát Hình 15.1, cho biết nồng độ của chất phản ứng và sản phẩm thay đổi như thế nào theo thời gian
|
Phương pháp giải:
Quan sát đồ thị và rút ra nhận xét
Lời giải chi tiết:
- Nồng độ chất phản ứng giảm dần theo thời gian
- Nồng độ chất sản phẩm tăng dần theo thời gian
CH tr 95 LT
|
Xét phản ứng phân hủy N 2 O 5 ở 45 o C N 2 O 5 (g) → N 2 O 4 (g) + ½ O 2 (g) Sau 184 giây đầu tiên, nồng độ của N 2 O 4 là 0,25M. Tính tốc độ trung bình của phản ứng theo N 2 O 4 trong khoảng thời gian trên |
Phương pháp giải:
aA + bB → cC + dD
Áp dụng công thức:
\(\mathop v\limits^\_ = - \frac{1}{a}\frac{{\Delta {C_A}}}{{\Delta t}} = - \frac{1}{b}\frac{{\Delta {C_B}}}{{\Delta t}} = \frac{1}{c}\frac{{\Delta {C_C}}}{{\Delta t}} = \frac{1}{d}\frac{{\Delta {C_D}}}{{\Delta t}}\)
Lời giải chi tiết:
Áp dụng công thức: \(\mathop v\limits^\_ = - \frac{1}{a}\frac{{\Delta {C_A}}}{{\Delta t}} = - \frac{1}{b}\frac{{\Delta {C_B}}}{{\Delta t}} = \frac{1}{c}\frac{{\Delta {C_C}}}{{\Delta t}} = \frac{1}{d}\frac{{\Delta {C_D}}}{{\Delta t}}\)
=> \(\mathop v\limits^\_ = \frac{1}{1}\frac{{\Delta {C_{{N_2}{O_4}}}}}{{\Delta t}} = \frac{1}{1}\frac{{0,25}}{{184}} = 1,{36.10^{ - 3}}(M/s)\)
Tốc độ trung bình của phản ứng theo N 2 O 4 trong 184 giây là 1,36.10 -3 (M/s)
CH tr 96 CH
|
4. Theo định luật tác dụng khối lượng, tốc độ phản ứng thay đổi như thế nào khi tăng hoặc giảm nồng độ chất phản ứng |
Phương pháp giải:
Định luật tác dụng khối lượng: Ở nhiệt độ không đổi, tốc độ phản ứng tỉ lệ với tích số nồng độ các chất tham gia phản ứng với số mũ thích hợp
Lời giải chi tiết:
Tốc độ phản ứng tỉ lệ thuận với nồng độ các chất tham gia phản ứng với số mũ thích hợp
=> Khi nồng độ tăng thì tốc độ phản ứng tăng và ngược lại
CH tr 96 CH
|
5. Trong tự nhiên và cuộc sống, có nhiều phản ứng hóa học xảy ra với tốc độ khác nhau phụ thuộc vào nồng độ chất phản ứng, tìm các ví dụ minh họa |
Phương pháp giải:
Ví dụ:
+ Que đóm còn tàn đỏ bùng cháy khi cho vào bình oxygen
+ Cho nhiều men vào bánh mì thì bánh mì lên men nhanh hơn
+ Làm sữa chua
Lời giải chi tiết:
- Khi cho que đóm còn tàn đỏ vào bình oxygen thì que đóm bùng cháy, để ở ngoài thì k hiện tượng là do nồng độ oxygen trong bình khí oxygen cao hơn
- Khi làm bánh mì, nếu cho nhiều men vào bột thì quá trình lên men diễn ra nhanh hơn
- Khi làm sữa chua, nếu cho nhiều sữa chua thì quá trình lên men diễn ra nhanh hơn
CH tr 96 LT
|
Cho phản ứng đơn giản sau: H 2 (g) + Cl 2 (g) → 2HCl(g) a) Viết biểu thức tốc độ tức thời của phản ứng trên b) Tốc độ phản ứng thay đổi thế nào khi nồng độ H 2 giảm 2 lần và giữ nguyên nồng độ Cl 2 ? |
Phương pháp giải:
a) v = k.C Cl2 .C H2
b) Áp dụng công thức tính tốc độ tức thời
Lời giải chi tiết:
a) Biểu thức tốc độ tức thời của phản ứng là:
v1 = k.C Cl2 .C H2
b) Gọi C Cl2 là nồng độ ban đầu của Cl, C H2 là nồng độ đầu của H 2
=> v2 = k. C Cl2 .C H2 :2
=> 2v2 = v1
=> Tốc độ phản ứng giảm 1 nửa khi nồng độ H 2 giảm 2 lần và giữ nguyên nồng độ Cl 2
CH tr 96 VD
|
Dưới đây là một số hiện tượng xảy ra trong đời sống, hãy sắp xếp theo thứ tự tốc độ giảm dần:
|
Lời giải chi tiết:
Sắp xếp theo thứ tự tốc độ giảm dần:
|
Đốt gas khi nấu ăn: vài giây |
(2) |
|
Nướng bánh mì: 2-3 phút |
(1) |
|
Lên men sữa tạo ra sữa chua: 1 ngày |
(3) |
|
Tấm tôn thiếc bị gỉ sét: 1 tháng |
(4) |
Bài tập 1
|
Bài 1: Cho phản ứng đơn giản xảy ra trong bình kín: 2NO(g) + O 2 (g) → 2NO 2 (g) a) Viết biểu thức tốc độ tức thời của phản ứng b) Ở nhiệt độ không đổi, tốc độ phản ứng thay đổi thế nào khi - nồng độ O 2 tăng 3 lần, nồng độ NO không đổi? - nồng độ NO tăng 3 lần, nồng độ O 2 không đổi? - nồng độ NO và O 2 đều tăng 3 lần? |
Phương pháp giải:
a) v = k.C NO 2 .C O2
b) Áp dụng công thức tính tốc độ tức thời
Lời giải chi tiết:
a) Công thức tính tốc độ tức thời của phản ứng là: v1 = k.C NO 2 .C O2
b)
- Nồng độ O 2 tăng 3 lần, nồng độ NO không đổi: v2 = k.C NO 2 .(C O2 .3)
=> v2 tăng 3 lần so với v1
- Nồng độ NO tăng 3 lần, nồng độ O 2 không đổi: v3 = k.(C NO .3) 2 .C O2 = k.C NO 2 .9.C O2
=> v3 tăng 9 lần so với v1
- Nồng độ NO và O 2 đều tăng 3 lần: v4 = k.(C NO .3) 2 .(C O2 .3) = k.C NO 2 .27.C O2
=> v4 tăng 27 lần so với v1
Bài tập 2
|
Bài 2: Giải thích tại sao tốc độ tiêu hao của NO (M/s) và tốc độ tạo thành của N 2 (M/s) không giống nhau trong phản ứng: 2CO(g) + 2NO(g) → 2CO 2 (g) + N 2 (g) |
Lời giải chi tiết:
Từ phương trình hóa học nhận thấy: hệ số cân bằng của NO là 2, hệ số cân bằng của N 2 là 1
=> Trong cùng thời gian, nồng độ tiêu hao của NO nhanh gấp 2 lần nồng độ tạo thành của N 2
Bài tập 3
|
Bài 3: Cho phản ứng: 2N 2 O 5 (g) → 4NO 2 (g) + O 2 (g) Sau thời gian từ giây 61 đến giây 120, nồng độ NO 2 tăng từ 0,30M lên 0,40M. Tính tốc độ trung bình của phản ứng |
Phương pháp giải:
Áp dụng công thức: \(\mathop v\limits^\_ = - \frac{1}{a}\frac{{\Delta {C_A}}}{{\Delta t}} = - \frac{1}{b}\frac{{\Delta {C_B}}}{{\Delta t}} = \frac{1}{c}\frac{{\Delta {C_C}}}{{\Delta t}} = \frac{1}{d}\frac{{\Delta {C_D}}}{{\Delta t}}\)
Lời giải chi tiết:
Vì NO 2 là chất sản phẩm
=> \(\mathop v\limits^\_ = \frac{1}{4}\frac{{\Delta {C_{N{O_2}}}}}{{\Delta t}} = \frac{1}{4}\frac{{0,4 - 0,3}}{{120 - 61}} = 4,{2.10^{ - 4}}(M/s)\)
Bài tập 4
|
Bài 4:
Dữ liệu thí nghiệm của phản ứng: SO
2
Cl
2
(g) → SO
2
(g) + Cl
2
(g) được trình bày ở bảng sau:
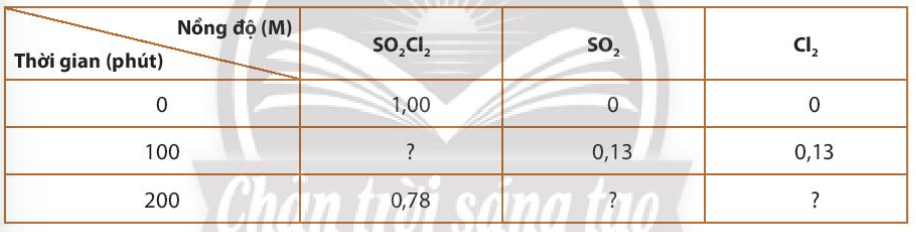
a) Tính tốc độ trung bình của phản ứng theo SO 2 Cl 2 trong thời gian 100 phút. b) Sau 100 phút, nồng độ của SO 2 Cl 2 còn lại là bao nhiêu c) Sau 200 phút, nồng độ của SO 2 và Cl 2 thu được là bao nhiêu? |
Phương pháp giải:
Áp dụng công thức: \(\mathop v\limits^\_ = - \frac{1}{a}\frac{{\Delta {C_A}}}{{\Delta t}} = - \frac{1}{b}\frac{{\Delta {C_B}}}{{\Delta t}} = \frac{1}{c}\frac{{\Delta {C_C}}}{{\Delta t}} = \frac{1}{d}\frac{{\Delta {C_D}}}{{\Delta t}}\)
Lời giải chi tiết:
a) Trong 100 phút, chất tạo thành từ 0M tăng lên 0,13M
=> ∆C = 0,13M
\(\mathop v\limits^\_ = \frac{1}{1}\frac{{\Delta {C_{S{O_2}C{l_{_2}}}}}}{{\Delta t}} = \frac{1}{1}\frac{{0,13}}{{100}} = 1,{3.10^{ - 3}}(M/phut)\)
b) Ta có: -∆C SO2Cl2 = 0,13M = 1,00 – C 2
=> C 2 = 0,87M
c) Sau 200 phút
-∆C SO2Cl2 = C 1 – C 2 = 1,00 – 0,78 = 0,22M
=> Sau 200 phút, nồng độ của SO 2 và Cl 2 = 0,22M