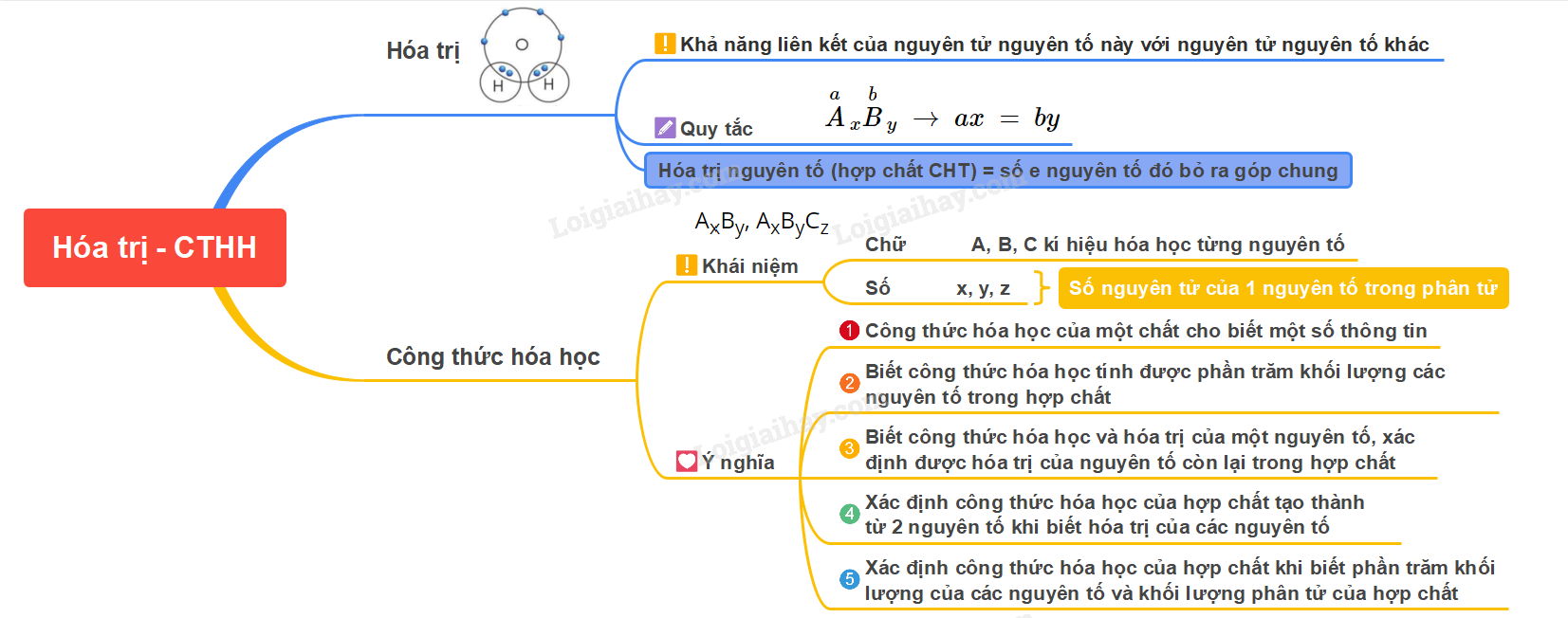
Lý thuyết bài 6: Hóa trị, công thức hóa học - KHTN 7 Cánh Diều
Hóa trị, công thức hóa học
Lý thuyết: Hóa trị, công thức hóa học
I. Hóa trị
1. Khái niệm về hóa trị
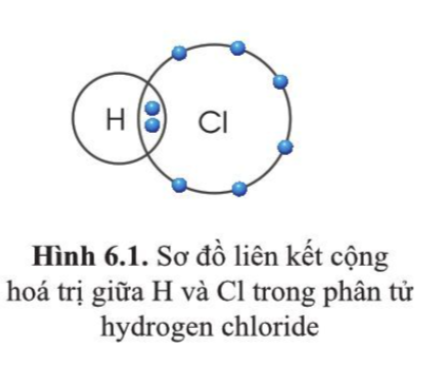
- Khi tạo thành phân tử hydrogen chloride, mỗi nguyên tử H và Cl góp 1 electron
=> Đôi electron dùng chung giữa 2 nguyên tử
=> H và Cl có hóa trị I
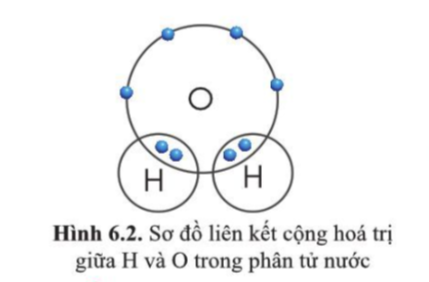
- Khi H kết hợp với O, mỗi nguyên tử H góp chung 1 electron, nguyên tử O góp chung 2 electron
=> H có hóa trị I, O có hóa trị II

- Hóa trị của nguyên tố trong hợp chất cộng hóa trị = số electron mà nguyên tử nguyên tố đó góp chung với nguyên tử khác
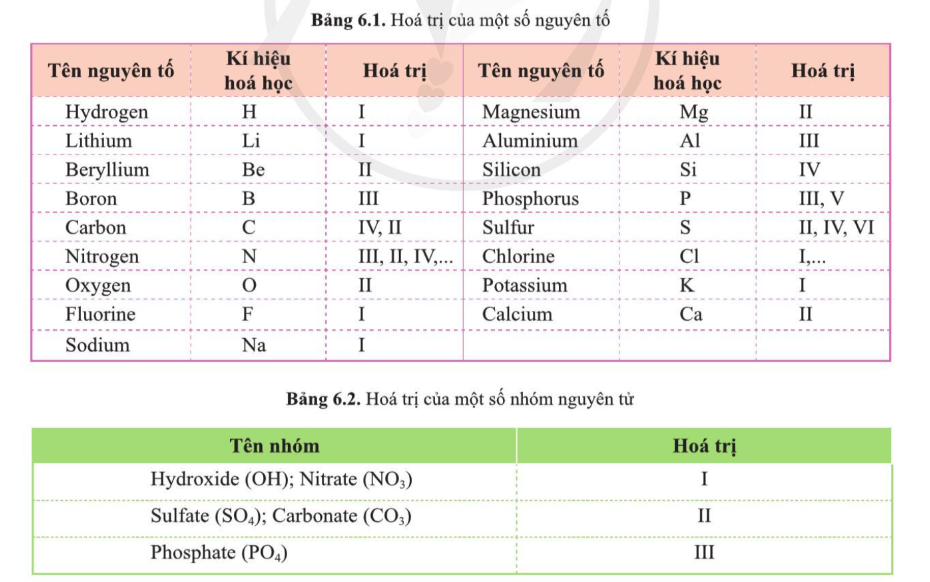
- Trong hợp chất, H luôn có hóa trị I, O luôn có hóa trị II
2. Quy tắc hóa trị

Ví dụ:
- Phân tử H 2 O
|
Nguyên tố |
H |
O |
|
Hóa trị |
I |
II |
|
Số nguyên tử |
2 |
1 |
|
Tích hóa trị và số nguyên tử |
I x 2 = II x 1 |
- Phân tử CO 2
|
Nguyên tố |
C |
O |
|
Hóa trị |
IV |
II |
|
Số nguyên tử |
1 |
2 |
|
Tích hóa trị và số nguyên tử |
IV x 1 = II x 2 |
II. Công thức hóa học
1. Công thức hóa học
- Công thức hóa học có 2 phần: phần chữ và phần số
+ Phần chữ: gồm kí hiệu hóa học của các nguyên tố tạo thành chất
+ Phần số: gồm các số được ghi bên phải, dưới chân kí hiệu hóa học, ứng với số nguyên tử của nguyên tố trong một phân tử (các số này được gọi là chỉ số)
Ví dụ: Công thức hóa học: H 2 O, NH 3 , CO 2
- Công thức hóa học của các đươn chất chỉ có 1 kí hiệu hóa học
+ Với phi kim, phân tử thường có 2 nguyên tử: N 2 , O 2 , H 2 …
+ Với kim loại và một số phi kim, kí hiệu hóa học của nguyên tố được coi là công thức hóa học của đơn chất. Ví dụ kim loại: Fe, Cu, Al… và một số phi kim như: C, S, P,…
- Công thức hóa học của các hợp chất có từ hai kí hiệu hóa học trở lên: NaCl, Na 2 O,…
2. Ý nghĩa của công thức hóa học
Công thức hóa học của một chất cho biết một số thông tin
- Nguyên tố tạo ra chất
- Số nguyên tử của mỗi nguyên tố có trong một phân tử chất
- Khối lượng phân tử của chất
Ví dụ: Công thức hóa học của H 2 SO 4 cho biết
- Sulfuric acid được tạo thành từ H, S và O
- Trong một phân tử sulfuric acid có 2 nguyên tử H, 1 nguyên tử S và 4 nguyên tử O
- Khối lượng phân tử: 2x1 + 1x32 + 4x16 = 98 (amu)
Biết công thức hóa học tính được phần trăm khối lượng các nguyên tố trong hợp chất
Bước 1: Tính khối lượng mỗi nguyên tố có trong một phân tử hợp chất
Bước 2: Tính khối lượng phân tử
Bước 3: Tính phần trăm khối lượng của nguyên tố theo công thức:
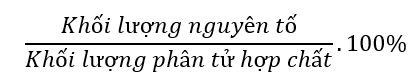
Ta có: Khối lượng của nguyên tố O trong MgO = 1 x 16 = 16 amu
Khối lượng của nguyên tố Mg trong MgO = 1 x 24 = 24 amu
=> Khối lượng phân tử MgO = 16 + 24 = 40 amu
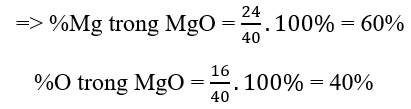
Biết công thức hóa học và hóa trị của một nguyên tố, xác định được hóa trị của nguyên tố còn lại trong hợp chất
Bước 1: Đặt hóa trị của nguyên tố chưa biết là a
Bước 2: Xác định a dựa vào quy tắc hóa trị
Ví dụ: Xác định háo trị của Fe trong hợp chất có công thức hóa học là Fe 2 O 3
Gọi hóa trị của Fe trong hợp chất là a
Vì O có hóa trị II nên khi áp dụng quy tắc hóa trị: a.2 = II.3 => a = III
Vậy Fe có hóa trị III trong hợp chất Fe 2 O 3
3. Xác định công thức hóa học của hợp chất khi biết hóa trị hoặc phần trăm khối lượng của các nguyên tố
Xác định công thức hóa học của hợp chất tạo thành từ 2 nguyên tố khi biết hóa trị của các nguyên tố

Xác định công thức hóa học của hợp chất khi biết phần trăm khối lượng của các nguyên tố và khối lượng phân tử của hợp chất
Bước 1: Đặt công thức hóa học của chất A x B y
Bước 2: Tính khối lượng của A, B trong một phân tử chất
Bước 3: Tìm x, y