Lý thuyết Hydrocarbon không no- Hóa học 11 - Cánh diều
Khái niệm, đồng phân và danh pháp-Tính chất vật lý-Tính chất hóa học-Ứng dụng và điều chế alkene, alkyne
Bài 13
HYDROCARBON KHÔNG NO
I.Khái niệm, đồng phân và danh pháp
1.Khái niệm
-Alkene là hydrocarbon không no, mạch hở, phân tử có một liên kết đôi (C=C), có công thức chung là C n H 2n (n≥2).
-Alkyne là hydrocarbon không no, mạch hở, phân tử có một liên kết ba (C≡C), có công thức chung là C n H 2n-2 (n≥2).
2.Đồng phân
-Alkene và alkyne có đồng phân cấu tạo gồm đồng phân về vị trí liên kết bội và đồng phân mạch carbon.
-Alkene còn có đồng phân hình học.
3.Danh pháp
-Tên của alkene và alkyne mạch không phân nhánh:
Tên tiền tố - số chỉ vị trí liên kết bội – tên hậu tố (ene/yne).
-Tên của alkene, alkyne có mạch chính được gọi như sau:
Số chỉ vị trí của mạch nhánh – tên mạch nhánh+tên tiền tố (mạch chính) – số chỉ vị trí liên kết bội – tên hậu tố.
II.Tính chất vật lý
-Ở điều kiện thường, các alkene, alkyne có số nguyên tử carbon nhỏ hơn 5 tồn tại ở thể khí.
-Đều ít tan trong nước nhưng tan tốt trong dung môi hữu cơ.
-Nhiệt độ nóng chảy, nhiệt độ sôi của alkene và alkyne đều tăng theo chiều tăng số nguyên tử carbon.
III.Tính chất hóa học
1.Phản ứng cộng
- Cộng hydrogen
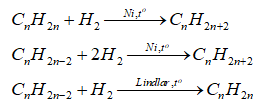
-Cộng halogen
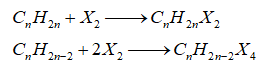
-Cộng hydrogen halide
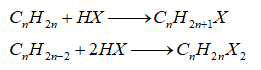
-Cộng nước (hydrate hóa)
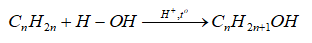
-Quy tắc Markovnikov: Nguyên tử hydrogen ưu tiên cộng vào nguyên tử carbon chưa no có nhiều hydrogen hơn, còn nguyên tử X ưu tiên cộng vào nguyên tử carbon chưa no có ít hydrogen hơn.
2.Phản ứng trùng hợp alkene
- Dưới áp suất, xúc tác và nhiệt độ thích hợp, các alkene tham gia phản ứng cộng liên tiếp các phân tử với nhau tạo phân tử polymer.
3.Phản ứng của alk-1-yne với dung dịch silver nitrate trong ammonia.
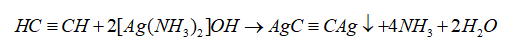
-Các alk-1-yne như ethyne, propyne,… có phản ứng tạo kết tủa với dung dịch AgNO 3 trong ammonia.
4.Phản ứng oxi hóa
a)Phản ứng với dung dịch potassium permanganate
- Alkene, alkyne đều bị oxi hóa bởi dung dịch KMnO 4 ở điều kiện thường
3C 2 H 4 + 2KMnO 4 + 4H 2 O 3C 2 H 4 (OH) 2 + 2KOH + 2MnO 2
3C 2 H 2 + 2KMnO 4 KOOC-COOK + 2KOH + 8MnO 2 + 2H 2 O
b)Phản ứng cháy
- Các alkene, alkyne cháy tỏa nhiều nhiệt:
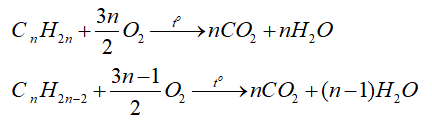
IV.Ứng dụng và điều chế alkene, alkyne
1.Ứng dụng
-Alkene là nguyên liệu để tổng hợp một số polymer như PE, PP,…
-Alkyne được dùng làm nguyên liệu cho tổng hợp hữu cơ.
-Ethylene và acetylene được dùng để làm chín trái cây, điều khiển quá trình sinh mủ của cây cao su.
-Đèn xì acetylene được sử dụng để hàn, cắt kim loại.
2.Điều chế
-Trong công nghiệp, alkene thường được điều chế từ phản ứng cracking alkane trong dầu mỏ.
-Alkene còn được điều chế bằng phản ứng tách nước từ alcohol:

-Acetylene được điều chế bằng cách cho calcium carbide tác dụng với nước:
CaC 2 + 2H 2 O C 2 H 2 + Ca(OH) 2
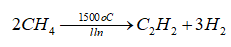
-Acetylene trong công nghiệp được sản xuất chủ yếu từ methane:
Sơ đồ tư duy về Hydrocarbon không no: