Đề thi học kì 2 Hóa 11 Cánh diều - Đề số 1
Cho alkyne X tác dụng với H2 dư
Đề bài
Dẫn xuất halogen X dưới đây:
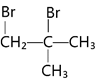
Có thể tạo thành từ phản ứng giữa bromine với chất nào dưới đây?
-
A.
but-2-ene.
-
B.
pent – 1 – ene.
-
C.
but-1-ene.
-
D.
2-methylpropene.
Alkene sau có tên gọi là:
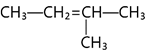
-
A.
2-methylbut-2-ene.
-
B.
3-methylbut-2-ene.
-
C.
2-metybut-3-ene.
-
D.
3-methylbut-3-ene.
Chất, dung dịch tác dụng với phenol sinh ra khí là
-
A.
dung dịch KOH.
-
B.
dung dịch \({{\rm{K}}_{\rm{2}}}{\rm{C}}{{\rm{O}}_{\rm{3}}}\).
-
C.
kim loại Na.
-
D.
kim loại Ag.
Cho alkyne X tác dụng với H 2 dư (xúc tác Lindlar) thu được duy nhất một sản phẩm hữu cơ Y có đồng phân hình học. Khi hydrogen hóa Y thì tạo thành 2-methylpentane. Tên gọi của X là
-
A.
2-methylpent-1-yne.
-
B.
2-methylpent-2-yne.
-
C.
4-methylpent-2-yne.
-
D.
4-methylpent-1-yne.
Phát biểu nào sau đây không đúng?
-
A.
Alcohol và phenol đều tham gia phản ứng với Na.
-
B.
Cho phenol phản ứng với dung dịch \({\rm{NaOH}}\), sau đó nhỏ vài giọt \({\rm{HCl}}\) vào dung dịch thì lại thu được phenol.
-
C.
Alcohol đa chức có nhóm \( - {\rm{OH}}\) liền kề phản ứng được với \({\rm{Cu}}{({\rm{OH}})_2}\) còn alcohol đơn chức thì không phản ứng.
-
D.
Đun nóng alcohol với H 2 SO 4 đặc chỉ thu được alkene.
Cồn \({70^ \circ }\) được sử dụng phổ biến trong y tế, dùng để sát trùng, diệt khuẩn,... Cách pha chế cồn \({70^ \circ }\) là
-
A.
pha \(70{\rm{\;mL}}\) nước với \(30{\rm{\;mL}}\) ethanol.
-
B.
pha \(70{\rm{\;mL}}\) ethanol với \(30{\rm{\;mL}}\) nước.
-
C.
lấy \(70{\rm{\;mL}}\) rồi thêm \(100{\rm{\;mL}}\) nước.
-
D.
lấy \(70{\rm{\;mL}}\) ethanol rồi thêm nước để thu được 100 mL cồn.
Nhận xét nào sau đây không đúng?
-
A.
Oxi hóa không hoàn toàn alcohol bậc I, thu được aldehyde
-
B.
Oxi hóa hoàn toàn alcohol bậc I, thu được aldehyde
-
C.
Oxi hóa alcohol bậc II, thu được ketone
-
D.
Alcohol bậc III không bị oxi hóa bởi tác nhân thông thường
Trong tinh dầu thảo mộc có những aldehyde không no tạo nên mùi thơm đặc trưng của tinh dầu. Ví dụ tinh dầu quế có aldehyde cinnamic C
6
H
5
CH=CHCHO có công thức cấu tạo là:

Tinh dầu sả và chanh có citronella C
9
H
17
CHO có công thức cấu tạo là:
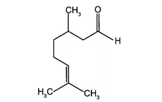
Hóa chất nào sau đây có thể dùng để nhận biết thành phần aldehyde trong tinh dầu?
-
A.
AgNO 3 /NH 3
-
B.
Dung dịch NaOH
-
C.
H 2 /Ni, t o
-
D.
Dung dịch HCl
Malic acid là thành phần chính tạo nên vị chua của quả táo, acid này có công thức cấu tạo như sau: HOOC-CH(OH)-CH 2 -COOH. Tên gọi của acid này là
-
A.
2-hydroxybutane-1,4-dioic acid.
-
B.
3-hydroxybutane-1,4-dioic acid.
-
C.
2,3-dihydroxybutanoic acid.
-
D.
2-hydroxypropane-1,2,3-tricarboxylic acid.
Khối lượng Ag thu được khi cho 0,1 mol CH 3 CHO phản ứng hoàn toàn với lượng dư dung dịch AgNO 3 trong NH 3 , đun nóng là
-
A.
21,6 gam.
-
B.
43,2 gam.
-
C.
16,2 gam.
-
D.
10,8 gam.
Cho 45 gam acetic acid phản ứng với 69 gam ethanol (xúc tác H 2 SO 4 đặc), đun nóng, thu được 41,25 gam ethyl acetate. Hiệu suất của phản ứng ester hoá là
-
A.
31,25%.
-
B.
40,00%.
-
C.
62,50%.
-
D.
50,00%.
Dãy gồm các chất được xếp theo chiều nhiệt độ sôi tăng dần từ trái sang phải là
-
A.
CH 3 CHO, C 2 H 5 OH, C 2 H 6 , CH 3 COOH.
-
B.
CH 3 COOH, C 2 H 6 , CH 3 CHO, C 2 H 5 OH.
-
C.
C 2 H 6 , C 2 H 5 OH, CH 3 CHO, CH 3 COOH.
-
D.
C 2 H 6 , CH 3 CHO, C 2 H 5 OH, CH 3 COOH.
Dữ liệu thực nghiệm của hợp chất hữu cơ X như sau:
- Kết quả phân tích nguyên tố của (X) có 40% C; 6,67% H; còn lại là O về khối lượng
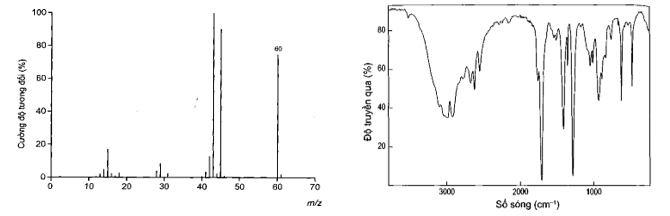
- Kết quả đo phổ khối lượng (MS) và phổ hồng ngoại (IR) của hợp chất (E) được cho như hình bên dưới:
(a) Công thức phân tử của X là C 2 H 4 O
(b) X có nhóm chức – CHO
(c) X có khả năng phản ứng với NaOH
(d) Trong phân tử X có 2 liên kết pi.
Chỉ số octane (octane number) là đại lượng đặc trưng cho yếu tố đo lường khả năng chống kích nổ của một nhiên liệu khi nhiên liệu này bốc cháy với không khí bên trong xi lanh của động cơ đốt trong. Nếu chỉ số octane của một mẫu xăng thấp, xăng sẽ tự cháy mà không do bu-gi bật tia lửa điện đốt. Điều này làm cho hiệu suất động cơ giảm và sẽ hư hao các chi tiết máy. Người ta quy ước rằng chỉ số octane của 2,2,4 – trimethylpentane là 100 và của heptane là 0. Các hydrocarbon mạch vòng và mạch phân nhánh có chỉ số octane cao hơn hydrocarbon mạch không nhánh.
(a) Chỉ số octane càng cao thì khả năng chịu nén của nhiên liệu trước khi phát nổ (đốt cháy) càng nhỏ, đồng thời giảm thiểu được ô nhiễm môi trường.
(b) Ethanol có thể làm tăng chỉ số octane của xăng
(c) Phản ứng reforming alkane được ứng dụng làm tăng chỉ số octane của xăng, dầu
(d) Một mẫu xăng chỉ gồm 8 phần thể tích 2,2,4 – trimethylpentane và 2 phần thể tích heptane thì chỉ số octane của mẫu xăng này là 60.
Cho các phát biểu:
(a) Do phân tử phân cực nên dẫn xuất halogen không tan trong dung môi hữu cơ như hydrocarbon, ether,..
(b) Nhiều dẫn xuất halogen có hoạt tính sinh học.
(c) Trong điều kiện thường, dẫn xuất halogen có thể ở dạng rắn, lỏng hay khí tùy thuộc vào khối lượng phân tử, bản chất và số lượng nguyên tử halogen.
(d) Nhiều dẫn xuất halogen được sử dụng trong tổng hợp các hợp chất hữu cơ.
Thí nghiệm được tiến hình như hình vẽ bên.
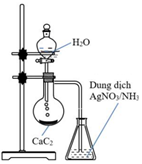
(a) Hiện tượng trong bình đựng dung dịch AgNO3/NH3 có xuất hiện kết tủa trắng bạc
(b) Thí nghiệm trên điều chế khí ethylene
(c) Sản phẩm có phản ứng làm mất màu dung dịch nước bromine
(d) CaC 2 có tên gọi khác là đất đèn.
Lời giải và đáp án
Dẫn xuất halogen X dưới đây:

Có thể tạo thành từ phản ứng giữa bromine với chất nào dưới đây?
-
A.
but-2-ene.
-
B.
pent – 1 – ene.
-
C.
but-1-ene.
-
D.
2-methylpropene.
Đáp án : D
Các hydrocarbon không no có phản ứng cộng với brmonie

Alkene sau có tên gọi là:
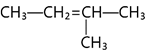
-
A.
2-methylbut-2-ene.
-
B.
3-methylbut-2-ene.
-
C.
2-metybut-3-ene.
-
D.
3-methylbut-3-ene.
Đáp án : A
Dựa vào quy tắc đọc tên của alkene

2 – methylbut – 2 – ene
Chất, dung dịch tác dụng với phenol sinh ra khí là
-
A.
dung dịch KOH.
-
B.
dung dịch \({{\rm{K}}_{\rm{2}}}{\rm{C}}{{\rm{O}}_{\rm{3}}}\).
-
C.
kim loại Na.
-
D.
kim loại Ag.
Đáp án : C
Dựa vào tính chất của phenol
Phenol tác dụng với kim loại Na tạo ra khí H 2 :
C 6 H 5 OH + Na \( \to \) C 6 H 5 ONa + ½ H 2
Đáp án C
Cho alkyne X tác dụng với H 2 dư (xúc tác Lindlar) thu được duy nhất một sản phẩm hữu cơ Y có đồng phân hình học. Khi hydrogen hóa Y thì tạo thành 2-methylpentane. Tên gọi của X là
-
A.
2-methylpent-1-yne.
-
B.
2-methylpent-2-yne.
-
C.
4-methylpent-2-yne.
-
D.
4-methylpent-1-yne.
Đáp án : C
Dựa vào cấu tạo của sản phẩm Y
Khi hydrogen hóa Y tạo thành 2 – methylpentane => Công thức cấu tạo Y là:
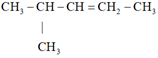
=> Công thức cấu tạo X:

Đáp án C
Phát biểu nào sau đây không đúng?
-
A.
Alcohol và phenol đều tham gia phản ứng với Na.
-
B.
Cho phenol phản ứng với dung dịch \({\rm{NaOH}}\), sau đó nhỏ vài giọt \({\rm{HCl}}\) vào dung dịch thì lại thu được phenol.
-
C.
Alcohol đa chức có nhóm \( - {\rm{OH}}\) liền kề phản ứng được với \({\rm{Cu}}{({\rm{OH}})_2}\) còn alcohol đơn chức thì không phản ứng.
-
D.
Đun nóng alcohol với H 2 SO 4 đặc chỉ thu được alkene.
Đáp án : D
Dựa vào tính chất của alcohol
Đun nóng alcohol với H 2 SO 4 đặc ở nhiệt độ 170 o C thu được alkene và ở nhiệt độ 140 o C thu được eter.
Đáp án D
Cồn \({70^ \circ }\) được sử dụng phổ biến trong y tế, dùng để sát trùng, diệt khuẩn,... Cách pha chế cồn \({70^ \circ }\) là
-
A.
pha \(70{\rm{\;mL}}\) nước với \(30{\rm{\;mL}}\) ethanol.
-
B.
pha \(70{\rm{\;mL}}\) ethanol với \(30{\rm{\;mL}}\) nước.
-
C.
lấy \(70{\rm{\;mL}}\) rồi thêm \(100{\rm{\;mL}}\) nước.
-
D.
lấy \(70{\rm{\;mL}}\) ethanol rồi thêm nước để thu được 100 mL cồn.
Đáp án : D
Dựa vào khái niệm độ cồn
Cồn 70 o chứa 70ml ethanol nên để pha được thì cần lấy 70 ml ethanol rồi thêm nước để thu được 100ml cồn.
Đáp án D
Nhận xét nào sau đây không đúng?
-
A.
Oxi hóa không hoàn toàn alcohol bậc I, thu được aldehyde
-
B.
Oxi hóa hoàn toàn alcohol bậc I, thu được aldehyde
-
C.
Oxi hóa alcohol bậc II, thu được ketone
-
D.
Alcohol bậc III không bị oxi hóa bởi tác nhân thông thường
Đáp án : B
Alcohol bậc III không bị oxi hóa bởi tác nhân thông thường
Oxi hóa hoàn toàn alcohol bậc I thu được CO 2 và H 2 O
Đáp án B
Trong tinh dầu thảo mộc có những aldehyde không no tạo nên mùi thơm đặc trưng của tinh dầu. Ví dụ tinh dầu quế có aldehyde cinnamic C
6
H
5
CH=CHCHO có công thức cấu tạo là:

Tinh dầu sả và chanh có citronella C
9
H
17
CHO có công thức cấu tạo là:

Hóa chất nào sau đây có thể dùng để nhận biết thành phần aldehyde trong tinh dầu?
-
A.
AgNO 3 /NH 3
-
B.
Dung dịch NaOH
-
C.
H 2 /Ni, t o
-
D.
Dung dịch HCl
Đáp án : A
Dựa vào tính chất hóa học của aldehyde
Aldehyde phản ứng tráng bạc với dung dịch AgNO 3 /NH 3
Đáp án A
Malic acid là thành phần chính tạo nên vị chua của quả táo, acid này có công thức cấu tạo như sau: HOOC-CH(OH)-CH 2 -COOH. Tên gọi của acid này là
-
A.
2-hydroxybutane-1,4-dioic acid.
-
B.
3-hydroxybutane-1,4-dioic acid.
-
C.
2,3-dihydroxybutanoic acid.
-
D.
2-hydroxypropane-1,2,3-tricarboxylic acid.
Đáp án : A
Dựa vào cách gọi tên của carboxylic acid
HOOC-CH(OH)-CH 2 -COOH: 2-hydroxybutane-1,4-dioic acid.
Đáp án A
Khối lượng Ag thu được khi cho 0,1 mol CH 3 CHO phản ứng hoàn toàn với lượng dư dung dịch AgNO 3 trong NH 3 , đun nóng là
-
A.
21,6 gam.
-
B.
43,2 gam.
-
C.
16,2 gam.
-
D.
10,8 gam.
Đáp án : A
1 mol CH 3 CHO khi phản ứng với AgNO 3 /NH 3 tạo ra 2 mol Ag
n CH3CHO = 0,1 mol => n Ag = 2.0,1 = 0,2 mol
=> m Ag = 0,2 . 108 = 21,6g
Đáp án A
Cho 45 gam acetic acid phản ứng với 69 gam ethanol (xúc tác H 2 SO 4 đặc), đun nóng, thu được 41,25 gam ethyl acetate. Hiệu suất của phản ứng ester hoá là
-
A.
31,25%.
-
B.
40,00%.
-
C.
62,50%.
-
D.
50,00%.
Đáp án : C
Dựa vào phản ứng ester hóa giữa carboxylic acid và alcohol.
n CH3COOH = 45 : 60 = 0,75 mol
n C2H5OH = 69 : 46 = 1,5 mol
n CH3COOC2H5 = 41,25 : 88 = 0,46875 mol
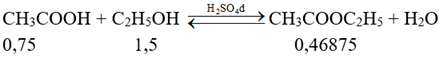
H% = \(\frac{{0,46875}}{{0,75}}.100 = 62,5\% \)
Đáp án C
Dãy gồm các chất được xếp theo chiều nhiệt độ sôi tăng dần từ trái sang phải là
-
A.
CH 3 CHO, C 2 H 5 OH, C 2 H 6 , CH 3 COOH.
-
B.
CH 3 COOH, C 2 H 6 , CH 3 CHO, C 2 H 5 OH.
-
C.
C 2 H 6 , C 2 H 5 OH, CH 3 CHO, CH 3 COOH.
-
D.
C 2 H 6 , CH 3 CHO, C 2 H 5 OH, CH 3 COOH.
Đáp án : D
Dựa vào liên kết hydrogen và tương tác van der Waals
C 2 H 6 < CH 3 CHO < C 2 H 5 OH < CH 3 COOH
Đáp án D
Dữ liệu thực nghiệm của hợp chất hữu cơ X như sau:
- Kết quả phân tích nguyên tố của (X) có 40% C; 6,67% H; còn lại là O về khối lượng
- Kết quả đo phổ khối lượng (MS) và phổ hồng ngoại (IR) của hợp chất (E) được cho như hình bên dưới:

(a) Công thức phân tử của X là C 2 H 4 O
(b) X có nhóm chức – CHO
(c) X có khả năng phản ứng với NaOH
(d) Trong phân tử X có 2 liên kết pi.
(a) Công thức phân tử của X là C 2 H 4 O
(b) X có nhóm chức – CHO
(c) X có khả năng phản ứng với NaOH
(d) Trong phân tử X có 2 liên kết pi.
Dựa vào phổ IR của X từ đó tìm công thức của X
%O = 100% - %C - %H = 100% - 40% - 6,67% = 53,33%
C : H : O = \(\frac{{\% C}}{{12}}:\frac{{\% H}}{1}:\frac{{\% O}}{{16}} = \frac{{40\% }}{{12}}:\frac{{6,67\% }}{1}:\frac{{53,33\% }}{{16}} = 3,33:6,67:3,33 = 1:2:1\)
Công thức đơn giản nhất là (CH 2 O) n
Theo phổ MS: M X = 60 => M(CH 2 O) n = 60 => n = 2 => X: C 2 H 4 O 2
Theo phổ IR: X có vùng tín hiệu đặc trưng ở 3000 – 2500 cm-1 và 1750 – 1680 cm-1. Đây là 2 vùng tín hiệu đặc trưng của nhóm – COOH.
(a) Sai vì công thức phân tử X là C 2 H 4 O 2
(b) Sai vì X có nhóm chức – COOH
(c) Đúng vì X là CH 3 COOH: acetic acid phản ứng với dung dịch NaOH
(d) Sai, trong phân tử X có 1 liên kết pi ( C=O)
Chỉ số octane (octane number) là đại lượng đặc trưng cho yếu tố đo lường khả năng chống kích nổ của một nhiên liệu khi nhiên liệu này bốc cháy với không khí bên trong xi lanh của động cơ đốt trong. Nếu chỉ số octane của một mẫu xăng thấp, xăng sẽ tự cháy mà không do bu-gi bật tia lửa điện đốt. Điều này làm cho hiệu suất động cơ giảm và sẽ hư hao các chi tiết máy. Người ta quy ước rằng chỉ số octane của 2,2,4 – trimethylpentane là 100 và của heptane là 0. Các hydrocarbon mạch vòng và mạch phân nhánh có chỉ số octane cao hơn hydrocarbon mạch không nhánh.
(a) Chỉ số octane càng cao thì khả năng chịu nén của nhiên liệu trước khi phát nổ (đốt cháy) càng nhỏ, đồng thời giảm thiểu được ô nhiễm môi trường.
(b) Ethanol có thể làm tăng chỉ số octane của xăng
(c) Phản ứng reforming alkane được ứng dụng làm tăng chỉ số octane của xăng, dầu
(d) Một mẫu xăng chỉ gồm 8 phần thể tích 2,2,4 – trimethylpentane và 2 phần thể tích heptane thì chỉ số octane của mẫu xăng này là 60.
(a) Chỉ số octane càng cao thì khả năng chịu nén của nhiên liệu trước khi phát nổ (đốt cháy) càng nhỏ, đồng thời giảm thiểu được ô nhiễm môi trường.
(b) Ethanol có thể làm tăng chỉ số octane của xăng
(c) Phản ứng reforming alkane được ứng dụng làm tăng chỉ số octane của xăng, dầu
(d) Một mẫu xăng chỉ gồm 8 phần thể tích 2,2,4 – trimethylpentane và 2 phần thể tích heptane thì chỉ số octane của mẫu xăng này là 60.
(a) Sai vì chỉ số octane càng cao thì khả năng chịu nén của nhiên liệu trước khi phát nổ càng nhỏ
(b) Đúng vì ethanol có chỉ số octane lớn hơn nhiều so với xăng
(c) Đúng vì phản ứng reforming tạo ra các hydrocarbon mạch phân nhánh làm tăng chỉ số octane của xăng, dầu
(d) Sai vì chỉ số octan của mẫu xăng này là 80.
Cho các phát biểu:
(a) Do phân tử phân cực nên dẫn xuất halogen không tan trong dung môi hữu cơ như hydrocarbon, ether,..
(b) Nhiều dẫn xuất halogen có hoạt tính sinh học.
(c) Trong điều kiện thường, dẫn xuất halogen có thể ở dạng rắn, lỏng hay khí tùy thuộc vào khối lượng phân tử, bản chất và số lượng nguyên tử halogen.
(d) Nhiều dẫn xuất halogen được sử dụng trong tổng hợp các hợp chất hữu cơ.
(a) Do phân tử phân cực nên dẫn xuất halogen không tan trong dung môi hữu cơ như hydrocarbon, ether,..
(b) Nhiều dẫn xuất halogen có hoạt tính sinh học.
(c) Trong điều kiện thường, dẫn xuất halogen có thể ở dạng rắn, lỏng hay khí tùy thuộc vào khối lượng phân tử, bản chất và số lượng nguyên tử halogen.
(d) Nhiều dẫn xuất halogen được sử dụng trong tổng hợp các hợp chất hữu cơ.
(a) Sai, dẫn xuất halogen tan được trong dung môi hữu cơ
(b) Đúng
(c) Đúng
(d) Đúng
Thí nghiệm được tiến hình như hình vẽ bên.

(a) Hiện tượng trong bình đựng dung dịch AgNO3/NH3 có xuất hiện kết tủa trắng bạc
(b) Thí nghiệm trên điều chế khí ethylene
(c) Sản phẩm có phản ứng làm mất màu dung dịch nước bromine
(d) CaC 2 có tên gọi khác là đất đèn.
(a) Hiện tượng trong bình đựng dung dịch AgNO3/NH3 có xuất hiện kết tủa trắng bạc
(b) Thí nghiệm trên điều chế khí ethylene
(c) Sản phẩm có phản ứng làm mất màu dung dịch nước bromine
(d) CaC 2 có tên gọi khác là đất đèn.
(a) Sai, hiện tượng trong bình đựng dung dịch AgNO 3 /NH 3 có xuất hiện kết tủa vàng nhạt.
(b) Thí nghiệm trên điều chế khí acetylene
(c) Đúng, acetylene có tham gia phản ứng cộng làm mất màu dung dịch nước bromine
(d) Đúng
C : H : O = \(\frac{{77,78}}{{12}}:\frac{{7,41}}{1}:\frac{{14,81}}{{16}} = 6,48:7,41:0,92 = 7:8:1\)
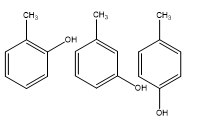
(a) Công thức phân tử A là: C7H8O
(b) Khi cho A vào ống nghiệm thêm dung dịch NaOH thấy A tan dần => A tác dụng được với NaOH
=> A thuộc hợp chất phenol. Vậy công thức cấu tạo của A là:
m NaOH = 100 . 10% = 10g
n NaOH = 10:40 = 0,25 mol
ta có: n – COOH = n NaOH = 0,25 mol
=> M Y = 11,5 : 0,4 = 46
Công thức cấu tạo của Y là: HCOOH
n HCHO = 3 : 30 = 0,1 mol
=> n Ag = 4 n HCHO = 0,1 . 4 = 0,4 mol
=> m Ag = 0,4 . 108 = 43,2g
Xăng có khối lượng riêng là 0,88 g/cm 3 nên 0,88 tấn xăng ứng với 1 m 3 . Vậy 88 tấn xăng ứng với 100 m 3 . Do đó trong 88 tấn xăng có pha trộn khoảng 100.1% = 1 m 3 benzene