Bài 18: Hợp chất carbonyl trang 115, 116, 117, 118, 119, 120, 121, 122, 123 Hóa học 11 Chân trời sáng tạo
Hợp chất carbonyl đơn giản nhất là aldehyde và ketone đơn chức. Chúng có nhiều ứng dụng trong ngành công nghiệp hóa chất cũng như trong thiên nhiên. Chẳng hạn, progesteron là hormon của nữ giới, 11-cis-retinal rất cần thiết cho khả năng nhìn của mắt. Hợp chất carbonyl là gì? Aldehyde và ketone có đặc điểm gì về tính chất vật lí và hoá học? Vai trò của chúng trong đời sống như thế nào?
CH tr 115 MĐ
Hợp chất carbonyl đơn giản nhất là aldehyde và ketone đơn chức. Chúng có nhiều ứng dụng trong ngành công nghiệp hóa chất cũng như trong thiên nhiên. Chẳng hạn, progesteron là hormon của nữ giới, 11-cis-retinal rất cần thiết cho khả năng nhìn của mắt. Hợp chất carbonyl là gì? Aldehyde và ketone có đặc điểm gì về tính chất vật lí và hoá học? Vai trò của chúng trong đời sống như thế nào?
Phương pháp giải:
Nêu khái niệm, tính chất vật lí, hóa học và ứng dụng của hợp chất carbonyl.
Lời giải chi tiết:
- Hợp chất carbonyl là các hợp chất hữu cơ trong phân tử có nhóm nhóm carbonyl. Aldehyde, ketone thuộc loại hợp chất carbonyl.
- Tính chất vật lí:
+ Formaldehyde và acetaldehyde là những chất khí ở nhiệt độ thường. Các hợp chất carbonyl khác là chất lỏng hoặc rắn.
+ Aldehyde, ketone có nhiệt độ sôi thấp hơn so với alcohol tương ứng nhưng cao hơn nhiều so với các hydrocarbon có phân tử khối tương đương.
+ Các aldehyde, ketone có mạch carbon ngắn dễ tan trong nước nhờ liên kết hydrogen với nước; các aldehyde, ketone có mạch carbon dài hơn ít tan hoặc không tan trong nước; các aldehyde, ketone thơm hầu như không tan.
+ Aldehyde, ketone thường có mùi đặc trưng.
- Tính chất hóa học: Phản ứng khử, phản ứng oxi hóa, phản ứng cộng, phản ứng tạo iodoform.
- Vai trò: Aldehyde và ketone có nhiều ứng dụng trong đời sống và sản xuất ở các lĩnh vực như: nông nghiệp, thủy sản, tổng hợp hữu cơ, sản xuất phẩm nhuộm,…
CH tr 116 CH 1
Quan sát Hình 18.1, nhận xét đặc điểm chung về cấu tạo của formaldehyde, acetaldehyde (aldehyde) và acetone (ketone). Hãy mô tả hình dạng phân tử của formaldehyde và acetaldehyde.
Phương pháp giải:
Formaldehyde, acetaldehyde (aldehyde) và acetone (ketone) đều là những hợp chất carbonyl.
Quan sát mô hình phân tử của formaldehyde và acetaldehyde, nêu ra hình dạng và các liên kết có trong các phân tử.
Lời giải chi tiết:
- Đặc điểm chung về cấu tạo của formaldehyde, acetaldehyde (aldehyde) và acetone (ketone): đều chứa nhóm carbonyl (>C=O).
- Hình dạng phân tử của formaldehyde và acetaldehyde:
+ Phân tử formaldehyde: gồm 1 nguyên tử carbon liên kết với 1 nguyên tử oxygen và 2 nguyên tử hydrogen, các nguyên tử đều nằm trên một mặt phẳng.
+ Phân tử acetaldehyde có 2 nguyên tử carbon liên kết với nhau, trong đó 1 nguyên tử carbon nằm ở tâm một hình tứ diện liên kết với 3 nguyên tử hydrogen, nguyên tử carbon còn lại liên kết với 1 nguyên tử oxygen và 1 nguyên tử hydrogen.
Hai phân tử trên có nhóm carbonyl, gồm nguyên tử carbon liên kết với nguyên tử oxygen bằng 1 liên kết σ bền và 1 liên kết π kém bền. Liên kết đôi C=O và 2 liên kết đơn nằm trên 1 mặt phẳng, góc liên kết khoảng 120°.
CH 116 LT
Viết công thức cấu tạo các đồng phân của hợp chất carbonyl có công thức phân tử C 4 H 8 O. Chất nào là aldehyde, chất nào là ketone?
Phương pháp giải:
Aldehyde là hợp chất hữu cơ trong phân tử có nhóm –CHO liên kết trực tiếp với nguyên tử carbon (của gốc hydrocarbon hoặc nhóm –CHO) hoặc nguyên tử hydrogen.
Ketone là hợp chất hữu cơ có nhóm carbonyl liên kết với 2 gốc hydrocarbon.
Lời giải chi tiết:
Đồng phân của hợp chất carbonyl có công thức phân tử C 4 H 8 O:
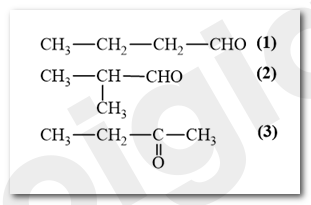
Công thức (1) và (2) là aldehyde.
Công thức (3) là ketone.
CH tr 117 CH 2
Dựa vào Bảng 18.1, rút ra cách gọi tên theo danh pháp thay thế của aldehyde so với ketone.
Phương pháp giải:
- Tên theo danh pháp thay thế của aldehyde đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + al
Đánh số các nguyên tử carbon ở mạch chính bắt đầu ở nguyên tử carbon của nhóm -CHO.
- Tên theo danh pháp thay thế của ketone đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + số chỉ vị trí nhóm carbonyl + one
Đánh số các nguyên tử carbon ở mạch chính bắt đầu từ nguyên tử carbon gần nhóm >C=O nhất.
Lời giải chi tiết:
- Cách gọi tên aldehyde theo danh pháp thay thế:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + al
- Danh pháp thay thế của ketone so với aldehyde: thêm số chỉ vị trí nhóm carbonyl (>C=O), thay hậu tố “al” bằng “one”.
CH tr 117 CH 3
Gọi tên theo danh pháp thay thế của các hợp chất carbonyl C 4 H 8 O đã viết ở trên.
Phương pháp giải:
- Tên theo danh pháp thay thế của aldehyde đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + al
Đánh số các nguyên tử carbon ở mạch chính bắt đầu ở nguyên tử carbon của nhóm -CHO.
- Tên theo danh pháp thay thế của ketone đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + số chỉ vị trí nhóm carbonyl + one
Đánh số các nguyên tử carbon ở mạch chính bắt đầu từ nguyên tử carbon gần nhóm >C=O nhất.
Lời giải chi tiết:

CH tr 117 LT
Gọi tên theo danh pháp thay thế của các hợp chất carbonyl sau:
a) (CH 3 ) 2 CHCHO
b) CH 3 CH 2 CH 2 COCH 3
c) CH 3 CH=C(CH 3 )CHO
Phương pháp giải:
- Tên theo danh pháp thay thế của aldehyde đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + al
Đánh số các nguyên tử carbon ở mạch chính bắt đầu ở nguyên tử carbon của nhóm -CHO.
- Tên theo danh pháp thay thế của ketone đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + số chỉ vị trí nhóm carbonyl + one
Đánh số các nguyên tử carbon ở mạch chính bắt đầu từ nguyên tử carbon gần nhóm >C=O nhất.
Lời giải chi tiết:
a) 2-methylpropanal.
b) pentan-2-one.
c) 2-methylbut-2-enal.
CH tr 117 LT
Viết công thức cấu tạo của các hợp chất sau:
a) 2-methylbutanal;
b) but-3-enal.
Phương pháp giải:
Từ cách gọi tên aldehyde (theo danh pháp thay thế) suy ra công thức cấu tạo.
Lời giải chi tiết:
a) CH3 - CH(CH3) - CH2 - CHO
b) CH2 = CH - CH2 - CHO
CH 117 VD
Tìm hiểu một số hợp chất carbonyl được tìm thấy trong thiên nhiên. Nêu vai trò của chúng trong đời sống.
Phương pháp giải:
Kể tên một số hợp chất carbonyl được tìm thấy trong thiên nhiên và nêu ứng dụng của các chất trên.
Lời giải chi tiết:
Các hợp chất carbonyl được tìm thấy trong thiên nhiên: cinnamaldehyde trong tinh dầu quế, vanillin hay methone trong tinh dầu bạc hà, citral trong tinh dầu xả…
Vì những hợp chất này có mùi thơm riêng biệt nên được sử dụng làm chất tạo hương trong công nghiệp thực phẩm và mĩ phẩm.
CH 118 CH 4
Dựa vào Bảng 18.2 hãy nhận xét sự thay đổi trạng thái, nhiệt độ sôi và độ tan của một số hợp chất carbonyl khi số nguyên tử carbon tăng dần.
Phương pháp giải:
+ Formaldehyde và acetaldehyde là những chất khí ở nhiệt độ thường. Các hợp chất carbonyl khác là chất lỏng hoặc rắn.
+ Aldehyde, ketone có nhiệt độ sôi thấp hơn so với alcohol tương ứng nhưng cao hơn nhiều so với các hydrocarbon có phân tử khối tương đương.
+ Các aldehyde, ketone có mạch carbon ngắn dễ tan trong nước nhờ liên kết hydrogen với nước; các aldehyde, ketone có mạch carbon dài hơn ít tan hoặc không tan trong nước; các aldehyde, ketone thơm hầu như không tan.
Lời giải chi tiết:
- Trạng thái: Formaldehyde và acetaldehyde là những chất khí ở nhiệt độ thường. Các hợp chất carbonyl khác là chất lỏng hoặc rắn.
- Nhiệt độ sôi của các hợp chất carbonyl tăng khi số nguyên tử carbon tăng dần.
- Độ tan của các hợp chất carbonyl giảm khi số nguyên tử carbon tăng dần.
CH 118 LT
Hãy sắp xếp theo thứ tự tăng dẫn nhiệt độ sôi các chất sau: acetaldehyde (1), ethanol (2), ethane (3). Giải thích.
Phương pháp giải:
Aldehyde, ketone có nhiệt độ sôi thấp hơn so với alcohol tương ứng. Các hợp chất carbonyl có nhiệt độ sôi cao hơn nhiều so với hydrocarbon có phân tử khối tương đương do phân tử chứa nhóm carbonyl phân cực làm phân tử các hợp chất carbonyl phân cực.
Các aldehyde, ketone có mạch carbon ngắn dễ tan trong nước nhờ có liên kết hydrogen với nước.
Lời giải chi tiết:
+ Các phân tử ethanol có liên kết hydrogen liên phân tử, do đó nhiệt độ sôi của ethanol lớn hơn so với các chất còn lại.
+ Acetaldehyde có nhiệt độ sôi cao hơn nhiều so với ethane vì acetaldehyde phân cực hơn ethane.
=> Nhiệt độ sôi của các chất được sắp xếp theo thứ tự tăng dần là: ethane (3), acetaldehyde (1), ethanol (2).
CH 118 VD
a) Formaldehyde là chất khí không màu, mùi hắc và gây khó chịu. Dung dịch trong nước, chứa khoảng 37% formaldehyde gọi là formalin. Hãy tìm hiểu ứng dụng của formalin sử dụng trong sinh học.
b) Ở nông thôn, nhiều gia đình vẫn đun bếp bằng rơm, rạ, hoặc củi. Tại sao rổ, rá, nong, nia, ... (được làm từ tre, nứa, giang. . . .) thường được gác lên gác bếp trước khi sử dụng để tăng độ bền của chúng?
Phương pháp giải:
a) Formalin được dùng để bảo quản các mẫu vật sinh học.
b) Formaldehyde có trong khói, có thể diệt trùng, chống mối mọt.
Lời giải chi tiết:
a) Formalin được dùng để bảo quản các mẫu vật sinh học.
b) Trong khói của bếp có chứa formaldehyde HCHO, chất này có khả năng diệt trùng, chống mối mọt nên làm rổ, rá, nong, nia, ... bền hơn.
CH 119 CH 5
Dựa vào giá trị độ âm điện của nguyên tử C và nguyên tử O, giải thích sự phân cực của liên kết C=O trong các hợp chất carbonyl.
Phương pháp giải:
Trong liên kết giữa nguyên tử A và B, nếu độ âm điện của nguyên tử A nhỏ hơn độ âm điện của nguyên tử B thì cặp electron dùng chung sẽ bị lệch về phía nguyên tử B. Nguyên tử B lúc này mang một phần điện tích âm (δ − ), nguyên tử A mang một phần điện tích dương (δ + ). Liên kết này gọi là liên kết cộng hóa trị có cực.
Lời giải chi tiết:
Giá trị độ âm điện của carbon và oxygen lần lượt là 2,55 và 3,44.
Do độ âm điện của nguyên tử oxygen lớn hơn nguyên tử carbon nên cặp electron dùng chung của liên kết C=O bị lệch về phía nguyên tử oxygen. Liên kết C=O phân cực về phía nguyên tử oxygen.
CH 119 LT
Viết sơ đồ phản ứng tạo thành alcohol của các chất sau (dùng chất khử là LiAlH 4 hoặc NaBH 4 ):
a) C 2 H 5 CHO
b) CH 3 COCH 2 CH 3
Phương pháp giải:
Các chất khử LiAlH 4 hoặc NaBH 4 khử aldehyde, ketone thành alcohol.
R-CHO R-CH 2 -OH
RCOR' R-CHOH-R'
Lời giải chi tiết:
a) C 2 H 5 CHO CH 3 -CH 2 -OH
b) CH 3 COCH 2 CH 3 CH 3 -CHOH- CH 2 CH 3
CH tr 119 CH 6
Cho biết sự thay đổi số oxi hoá của C và Br trong phương trình hoá học ở Ví dụ 4. Từ đó xác định chất oxi hoá và chất khử.
Phương pháp giải:
Trong phản ứng oxi hóa – khử, chất oxi hóa sau phản ứng có số oxi giảm, chất khử sau phản ứng có số oxi hóa tăng.
Lời giải chi tiết:
\({\rm{C}}{{\rm{H}}_{\rm{3}}}\mathop {\rm{C}}\limits^{ + 1} {\rm{H = O + }}{\mathop {{\rm{Br}}}\limits^0 _{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{C}}{{\rm{H}}_{\rm{3}}}\mathop {\rm{C}}\limits^{ + 3} {\rm{OOH + 2H}}\mathop {{\rm{Br}}}\limits^{ - 1} \)
Trong phản ứng trên, số oxi hoá của C (trong nhóm chức –CHO) tăng từ +1 lên +3, CH 3 CHO là chất oxi hóa. Số oxi hóa của Br giảm từ 0 xuống -1 , Br 2 là chất oxi hóa.
CH tr 120 CH 7
Xác định vai trò của CH 3 CHO trong phản ứng tráng bạc. Tìm hiểu ứng dụng của phản ứng trong thực tiễn.
Phương pháp giải:
Trong phản ứng oxi hóa – khử, chất oxi hóa sau phản ứng có số oxi giảm, chất khử sau phản ứng có số oxi hóa tăng.
Phản ứng tráng bạc được sử dụng trong công nghiệp tráng gương, tráng ruột phích.
Lời giải chi tiết:
- Trong phản ứng tráng bạc, số oxi hoá của C (trong nhóm chức –CHO) tăng từ +1 lên +3, do đó CH 3 CHO là chất khử.
- Ứng dụng: Phản ứng tráng bạc được sử dụng trong công nghiệp tráng gương, tráng ruột phích.
CH tr 120 CH 8
Vì sao trong phản ứng tráng bạc, người ta chỉ làm nóng mà không đun sôi hỗn hợp chất phản ứng?
Phương pháp giải:
Ở nhiệt độ cao, tốc độ phản ứng tăng.
Phức bạc (Ag(NH 3 ) 2 )OH dễ bị phân hủy ở nhiệt độ cao.
Lời giải chi tiết:
Nhiệt độ cao sẽ làm tăng tốc độ phản ứng quá nhanh, không kiểm soát được, quá trình tráng bạc diễn ra không đồng đều, khó tạo được lớp tráng mỏng và đồng nhất. Nhiệt độ cao làm phân hủy phức chất bạc (Ag(NH 3 ) 2 )OH tạo ra trong quá trình phản ứng, ảnh hưởng đến hiệu suất kết tủa bạc.
CH tr 120 CH 9
Khi cho dung dịch NaOH vào dung dịch CuSO 4 đến khi kết tủa không tăng thêm nữa, cho biết tên gọi và màu sắc của kết tủa thu được.
Phương pháp giải:
Người ta điều chế Cu(OH) 2 bằng dung dịch NaOH vào dung dịch CuSO 4 .
Lời giải chi tiết:
Khi cho dung dịch NaOH vào dung dịch CuSO 4 đến khi kết tủa không tăng thêm nữa, ta thu được kết tủa xanh lam Cu(OH) 2 – Copper(II) hydroxide.
2NaOH + CuSO 4 → Cu(OH) 2 ↓ + Na 2 SO 4
CH 121 LT
Trình bày phương pháp hoá học để nhận biết 3 chất lỏng riêng biệt sau: propan-1-ol (CH 3 CH 2 CH 2 OH), propanal (CH 3 CH 2 CHO) và acetone (CH 3 COCH 3 ).
Phương pháp giải:
Aldehyde làm mất màu nước bromine.
Alcohol bậc I bị oxi hóa bởi CuO (t o ).
Lời giải chi tiết:
- Đánh số thứ tự cho từng chất lỏng. Trích các chất lỏng làm mẫu thử đánh số thứ tự tương ứng.
- Nhỏ vài giọt nước bromine vào 3 mẫu thử:
+ Mẫu thử làm mất màu nước bromine là propanal: \({\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_2}{\rm{CH = O + B}}{{\rm{r}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{C}}{{\rm{H}}_2}{\rm{COOH + 2HBr}}\)
+ Hai mẫu thử không làm mất màu nước bromine là propan-1-ol, acetone.
- Tiếp tục trích mẫu thử của hai chất lỏng không làm mất màu nước bromine.
- Nung nóng dây đồng đỏ trên ngọn lửa đèn cồn đến khi dây đồng chuyển thành màu đen;
- Đưa dây đồng đen vào hai mẫu thử:
+ Mẫu thử làm dây đồng đen chuyển thành màu đỏ gạch chứa propan-1-ol.

+ Mẫu thử không làm dây đồng đen chuyển màu là acetone.
CH tr 121 CH 10
Từ đặc điểm cấu tạo nào của aldehyde, ketone chứng tỏ chúng có thể tham gia phản ứng cộng?
Phương pháp giải:
Phản ứng cộng là phản ứng hóa học, trong đó phân tử của một chất cộng vào kiên kết đôi hoặc liên kết ba trong phân tử của chất khác.
Lời giải chi tiết:
Aldehyde, ketone có phản ứng cộng xảy ra ở liên kết π kém bền của liên kết C=O.
CH tr 121 CH 11
Thực hiện Thí nghiệm 3 tạo iodoformn. Từ phương trình hoá học, xác định vai trò của I 2 và NaOH trong phản ứng tạo iodoform.
Phương pháp giải:
Các aldehyde và ketone có nhóm methyl cạnh nhóm carbonyl (CH 3 CO-) tham gia được phản ứng tạo iodoform.
Lời giải chi tiết:
CH 3 CHO + 3I 2 +4NaOH → H-COONa+ 3NaI + CHI 3 ↓ + 3H 2 O
Trong phản ứng trên, I 2 là chất oxi hóa (số oxi hóa của Igiảm từ 0 xuống -1), NaOH là môi trường.
CH tr 121 LT
Hoàn thành các phương trình hoá học của các phản ứng sau:
a) HCHO + (Ag(NH 3 ) 2 )OH →
b) C 2 H 5 CHO + Cu(OH) 2 + NaOH →
c) C 2 H 5 CHO + HCN →
Phương pháp giải:
a) Phản ứng tráng bạc của aldehyde: RCH=O + 2(Ag(NH 3 ) 2 )OH RCOONH 4 + 2Ag + 3NH 3 + H 2 O
b) Phản ứng oxi hóa aldehyde: RCHO + 2Cu(OH) 2 + NaOH RCOONa + Cu 2 O + 3H 2 O
c) Phản ứng cộng vào nhóm carbonyl của aldehyde: R-CH=O + HCN → R-CH(CN)-OH
Lời giải chi tiết:
a) HCHO + 4(Ag(NH 3 ) 2 )OH (NH 4 ) 2 CO 3 +4Ag + 6NH 3 + 2H 2 O
b) C 2 H 5 CHO + Cu(OH) 2 + NaOH C 2 H 5 COONa + Cu 2 O + 3H 2 O
c) C 2 H 5 CH=O + HCN → C 2 H 5 -CH(CN)-OH
CH tr 122 LT
Cho các hợp chất sau: methanal, pentan-3-one, butanone. Hợp chất nào trong các chất trên tham gia được phản ứng tạo iodoform? Giải thích.
Phương pháp giải:
Các aldehyde và ketone có nhóm methyl cạnh nhóm carbonyl (CH 3 CO-) tham gia được phản ứng tạo iodoform.
Lời giải chi tiết:
Các aldehyde và ketone có nhóm methyl cạnh nhóm carbonyl (CH 3 CO-) tham gia được phản ứng tạo iodoform, do đó chất có phản ứng tạo iodoform là: butanone (CH 3 CO-CH 2 CH 3 ).
CH tr 122 CH 12
Đọc thông tin về những ứng dụng của một số hợp chất carbonyl thường gặp, trình bày các ứng dụng của formaldehyde, acetaldehyde và acetone.
Phương pháp giải:
Nêu ứng dụng của formaldehyde, acetaldehyde và acetone.
Lời giải chi tiết:
- Formaldehyde: ứng dụng trong công nghiệp dệt, nhựa, chất dẻo, xây dựng, mỹ phẩm, keo dán, thuốc nổ, giấy than, mực máy photocopy, ... Ngoài ra, formaldehyde được sử dụng trong nông nghiệp và thuỷ sản.
- Acetaldehyde được dùng nhiều trong tổng hợp hữu cơ. Ví dụ sản xuất acetic acid, acetic anhydride, butanol, ...
- Acetone là dung môi tốt trong sản xuất tơ nhân tạo, thuốc súng không khói, dùng để pha loãng nhựa polyester và được sử dụng trong các chất tẩy rửa. Acetone là nguyên liệu để tổng hợp nhiều chất hữu cơ như chloroform, iodoform, methyl methacrylate, thuốc an thần sulfonal, ...
CH tr 122 VD
Vì sao acetone được dùng làm dung môi để lau sơn móng tay?
Phương pháp giải:
Acetone là dung môi hòa tan được nhiều hợp chất hữu cơ.
Lời giải chi tiết:
Acetone được dùng làm dung môi để lau sơn móng tay vì acetone dễ bay hơi và hòa tan được sơn móng tay.
Bài tập Bài 1
Hoàn thành thông tin còn thiếu vào bảng theo mẫu sau:
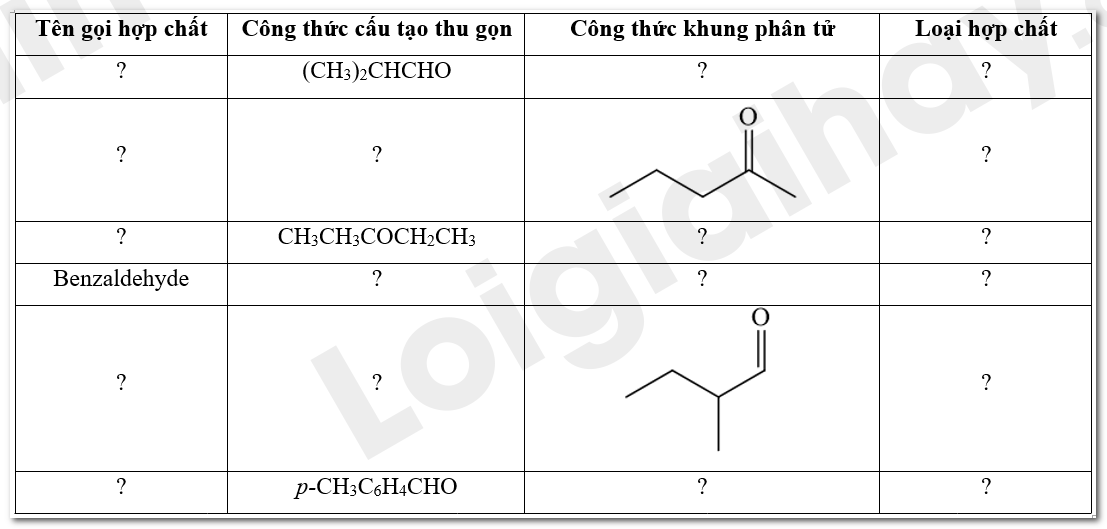
Phương pháp giải:
- Aldehyde là hợp chất hữu cơ trong phân tử có nhóm –CHO liên kết trực tiếp với nguyên tử carbon (của gốc hydrocarbon hoặc nhóm –CHO) hoặc nguyên tử hydrogen.
Ketone là hợp chất hữu cơ có nhóm carbonyl liên kết với 2 gốc hydrocarbon.
- Danh pháp:
+ Tên theo danh pháp thay thế của aldehyde đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + al
+ Tên theo danh pháp thay thế của ketone đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + số chỉ vị trí nhóm carbonyl + one
Lời giải chi tiết:
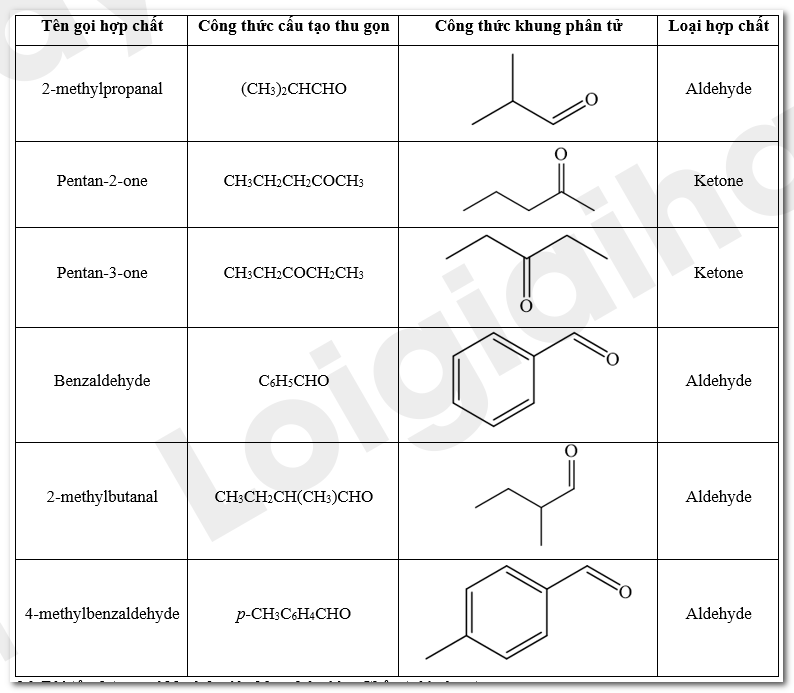
Bài tập Bài 2
Cho các chất sau: (1) C 3 H 8 , (2) C 2 H 5 OH, (3) CH 3 CHO. Sắp xếp các chất theo chiều tăng dẫn nhiệt độ sôi và độ tan trong nước. Giải thích.
Phương pháp giải:
Aldehyde, ketone có nhiệt độ sôi thấp hơn so với alcohol tương ứng. Các hợp chất carbonyl có nhiệt độ sôi cao hơn nhiều so với hydrocarbon có phân tử khối tương đương do phân tử chứa nhóm carbonyl phân cực làm phân tử các hợp chất carbonyl phân cực.
Các aldehyde, ketone có mạch carbon ngắn dễ tan trong nước nhờ có liên kết hydrogen với nước.
Lời giải chi tiết:
- Nhiệt độ sôi:
+ Các phân tử ethanol có liên kết hydrogen liên phân tử, do đó nhiệt độ sôi của ethanol lớn hơn so với các chất còn lại.
+ Acetaldehyde có nhiệt độ sôi cao hơn nhiều so với propane vì acetaldehyde phân cực hơn propane.
=> Nhiệt độ sôi của các chất được sắp xếp theo thứ tự tăng dần là: (1) C 3 H 8 , (3) CH 3 CHO, (2) C 2 H 5 OH.
- Độ tan trong nước:
+ Các phân tử ethanol hay acetaldehyde đều tạo liên kết hydrogen với nước, do đó ethanol và acetaldehyde đều tan vô hạn trong nước.
+ Propane không tạo liên kết hydrogen với nước, phân tử propane không phân cực, do đó propane không tan trong nước.
=> Độ tan trong nước của các chất được sắp xếp theo thứ tự tăng dần là: (1) C 3 H 8 , (3) CH 3 CHO, (2) C 2 H 5 OH.
Bài tập Bài 3
Viết công thức cấu tạo các hợp chất carbonyl có công thức phân tử C 5 H 10 O. Gọi tên theo danh pháp thay thế và tên thông thường (nếu có) của các đồng phân.
Phương pháp giải:
- Aldehyde là hợp chất hữu cơ trong phân tử có nhóm –CHO liên kết trực tiếp với nguyên tử carbon (của gốc hydrocarbon hoặc nhóm –CHO) hoặc nguyên tử hydrogen.
Ketone là hợp chất hữu cơ có nhóm carbonyl liên kết với 2 gốc hydrocarbon.
- Danh pháp:
+ Tên theo danh pháp thay thế của aldehyde đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + al
+ Tên theo danh pháp thay thế của ketone đơn chức mạch hở:
Tên hydrocarbon tương ứng (bỏ kí tự e ở cuối) + số chỉ vị trí nhóm carbonyl + one
Lời giải chi tiết:
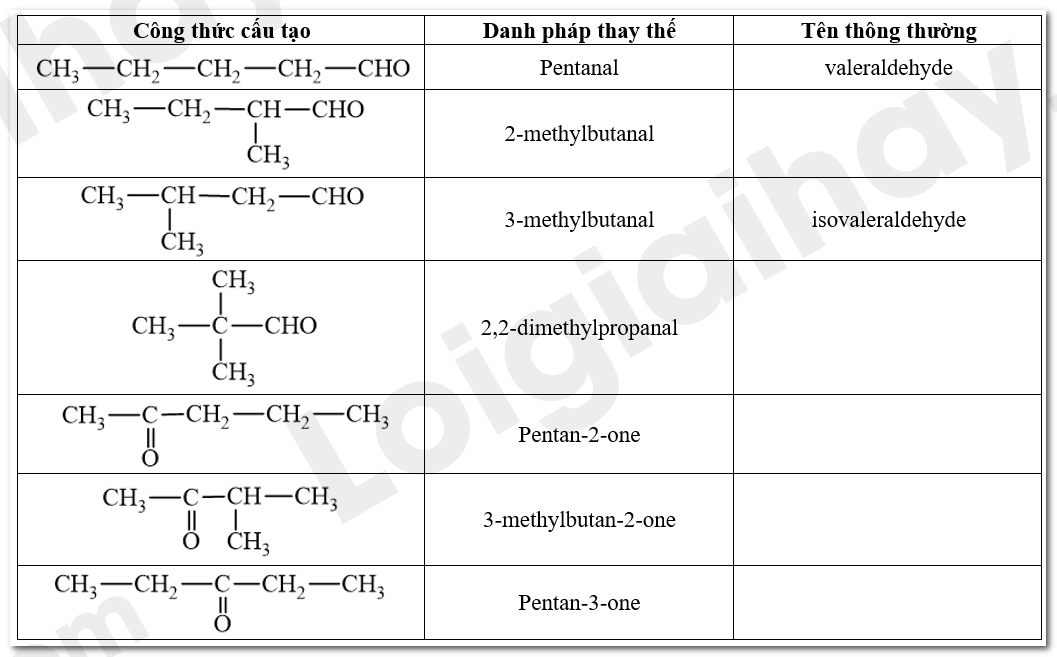
Bài tập Bài 4
Khi đo phổ IR của hợp chất X thu được kết quả ở hình dưới:
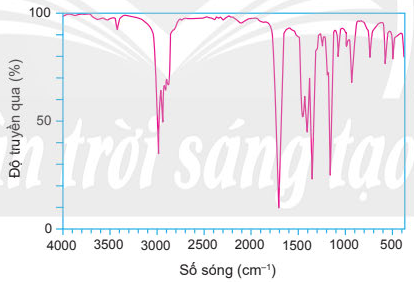
Bằng phương pháp phân tích nguyên tổ, xác định được thành phần các nguyên tố của hợp chất X chứa 66,66 %C, 11,11 %H về khối lượng, còn lại là O. Trên phổ MS của X, có peak ion phân tử (M') có giá trị m/z bằng 72. Chất X bị khử bởi LiAlH 4 tạo thành alcohol bậc II. Xác định công thức cấu tạo của X.
Phương pháp giải:
Dựa vào phổ IR, tìm các peak của nhóm chức. Tìm công thức phân tử từ phần trăm các nguyên tố và phân tử khối (kết quả phổ MS).
Ketone bị khử bởi LiAlH 4 tạo thành alcohol bậc II.
Lời giải chi tiết:
Gọi công thức đơn giản nhất của X là C x H y O z
%O = 100% - (66,66% + 11,11%) = 22,23%
Ta có:
\(\begin{array}{l}{\rm{x : y : z = }}\frac{{{\rm{\% C}}}}{{{\rm{12}}}}{\rm{ : }}\frac{{{\rm{\% H}}}}{{\rm{1}}}{\rm{ : }}\frac{{{\rm{\% O}}}}{{{\rm{16}}}}\\{\rm{ = }}\frac{{{\rm{66,66}}}}{{{\rm{12}}}}{\rm{ : }}\frac{{{\rm{11,11}}}}{{\rm{1}}}{\rm{ : }}\frac{{{\rm{22,23}}}}{{{\rm{16}}}} \approx 5,56:11,11:1,39 \approx 4:8:1\end{array}\)
=> Công thức đơn giản nhất của X là C 4 H 8 O.
=> Công thức phân tử của X có dạng (C 4 H 8 O) n
Dựa vào kết quả phổ MS của X, phân tử khối của X là 72.
Ta có: (12.4 + 1.8 + 16)n = 72 ó 72n = 72 => \({\rm{n = }}\frac{{72}}{{72}}{\rm{ = 1}}\)
=> Công thức phân tử của X là C 4 H 8 O.
Vì phổ IR của X có một peak trong vùng 1 670 – 1 740 cm -1 nên X có nhóm carbonyl.
Vì X bị khử bởi LiAlH 4 tạo thành alcohol bậc II nên X là ketone.
=> Công thức cấu tạo của X là: CH 3 CH 2 COCH 3 .