Lý thuyết mol và tỉ khối chất khí - Khoa học tự nhiên 8 - Kết nối tri thức
Mol là lượng chất có chứa NA (6,022.10-23) nguyên tử hoặc phân tử của chất đó.
I. Mol
1. Khái niệm
- Mol là lượng chất có chứa N A (6,022.10 -23 ) nguyên tử hoặc phân tử của chất đó.
- N A = 6,022.10 -23 là số Avogadro.
2. Khối lượng mol
- Kí hiệu: M
- Khối lượng mol của một chất là khối lượng của N A nguyên tử hoặc phân tử chất đó tính theo đơn vị gam.
- Công thức tính khối lượng mol: (với n là số mol chất có trong m gam)
3. Thể tích mol của chất khí
- Thể tích mol của chất khí là thể tích chiếm bởi N A phân tử của chất khí đó.
- Ở điều kiện chuẩn (25 o C và 1 bar), 1mol khí đều chiếm 24,79 lít.
→ V = n.24,79 (L)
II. Tỉ khối chất khí
- Để xác định khí A nặng hay nhẹ hơn bao nhiêu lần, người ta dựa vào tỉ số khối lượng mol của khí A (M A ) và khối lượng mol khí B (M B ).
- Công thức: d A/B = M A /M B .
- Tỉ khối của khí A so với không khí: d A/kk = M A /29.
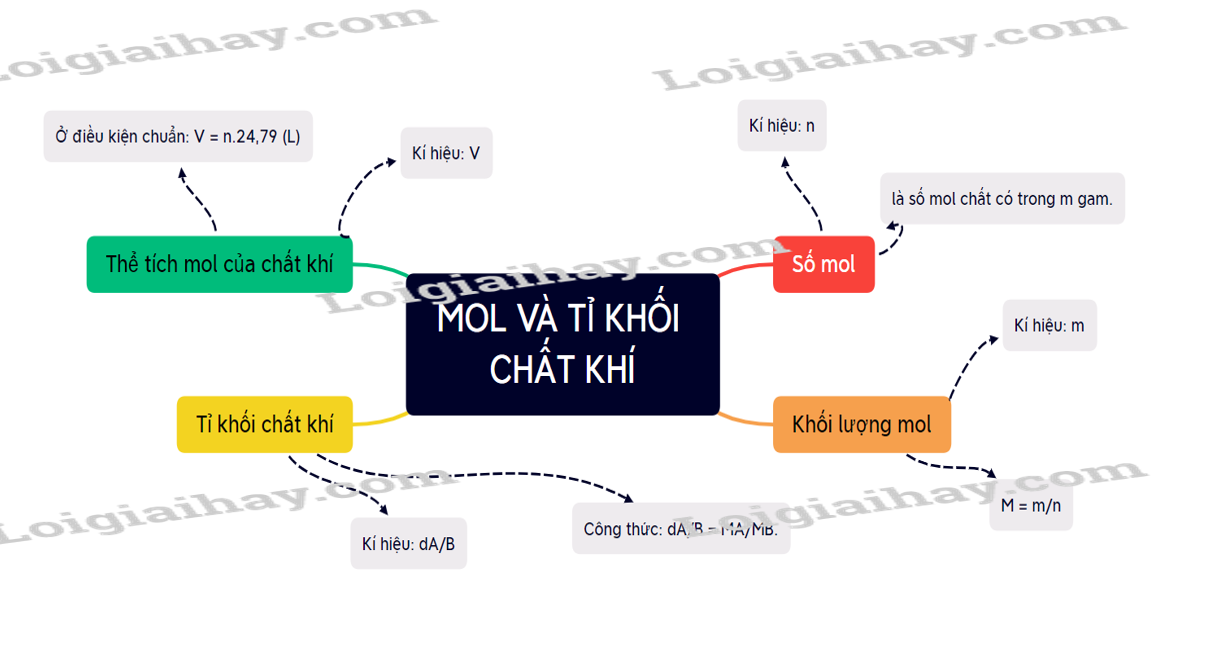
Sơ đồ tư duy