Lý thuyết pH của dung dịch. Chuẩn độ acid - base - Hóa học 11 - Cánh diều
- Môi trường acid có pH < 7. - Môi trường base có pH > 7. - Môi trường trung tính có pH = 7.
I. pH của dung dịch, chất chỉ thị
1. pH của dung dịch
|
pH = -lg[H + ] hoặc [H + ] = 10 -pH |
với [H + ] là nồng độ mol của ion H + .
- Môi trường acid có pH < 7.
- Môi trường base có pH > 7.
- Môi trường trung tính có pH = 7.
2. Ý nghĩa của pH trong thực tiễn
- pH có ý nghĩa trong tự nhiên, trong sản xuất và trong cơ thể sống xảy ra trong dung dịch nước với sự có mặt của các acid – base.
3. Xác định pH bằng chất chỉ thị
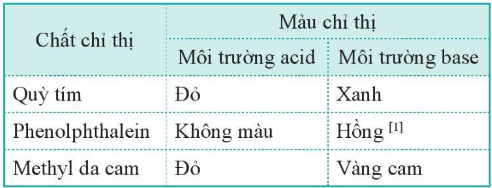
II. Chuẩn độ dung dịch acid và base
Nguyên tắc: Chuẩn độ là phương pháp xác định nồng độ của một chất bằng một dung dịch chuẩn đã biết nồng độ.
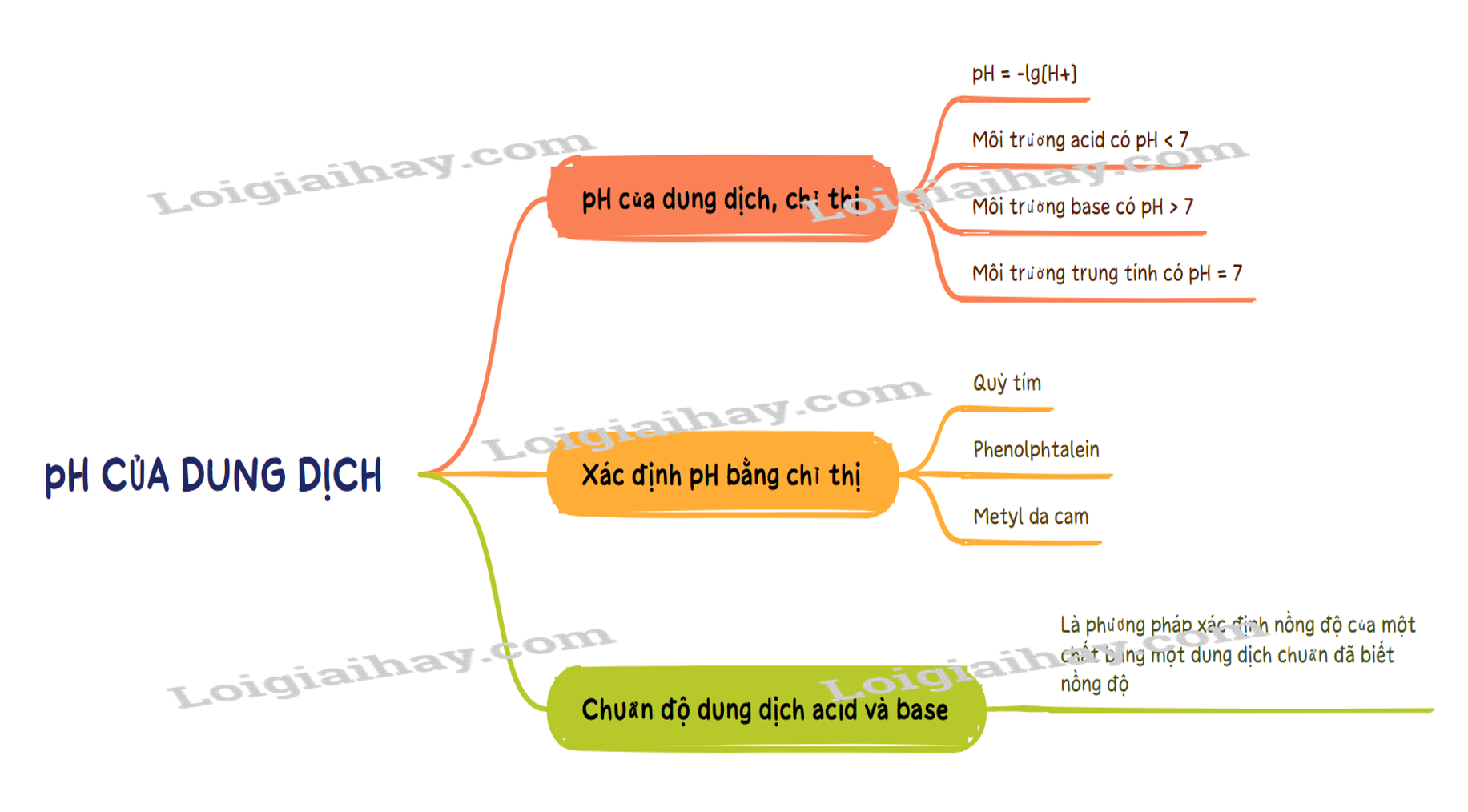
SƠ ĐỒ TƯ DUY
Cùng chủ đề:
Lý thuyết pH của dung dịch. Chuẩn độ acid - Base - Hóa học 11 - Cánh diều