Lý thuyết bài 13: Phản ứng oxi hóa - khử
Phản ứng oxi hóa - khử
Lý thuyết: Phản ứng oxi hóa - khử
I. Số oxi hóa
1. Khái niệm số oxi hóa
Số oxi hóa của một nguyên tử một nguyên tố trong hợp chất là điện tích của nguyên tử nguyên tố đó với giả định đây là hợp chất ion.
Ví dụ:
NaCl: số oxi hóa của Na là +1, của Cl là -1
MgO: số oxi hóa của Mg là +2, của O là -2
2. Cách xác định số oxi hóa của nguyên tử các nguyên tố trong hợp chất
Có 2 cách:
Cách 1: Dựa theo số oxi hóa của một số nguyên tử đã biết và điện tích của phân tử hoặc ion.
Quy tắc 1:
- Số oxi hóa của nguyên tử nguyên tố trong đơn chất bằng 0.
- Trong hợp chất, sô oxi hóa của H là +1, của O là -2, các kim loại kiềm (nhóm IA) là +1, kiềm thổ là +2, của Nhôm là +3.
Quy tắc 2:
Tổng số oxi hóa của các nguyên tử trong phân tử bằng 0, trong một ion đa nguyên tử bằng chính điện tích của ion đó.

Cách 2: Dựa theo công thức cấu tạo:
Ví dụ: CO 2 có CTCT: O=C=O
=> số oxi hóa của C là +4 và O là -2
II. Phản ứng oxi hóa khử:
1. Một số khái niệm
Phản ứng oxi hóa – khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của ít nhất một nguyên tố hóa học
- Chất khử (chất bị oxi hóa) là chất nhường electron.
- Chất oxi hóa (chất bị khử) là chất nhận electron
- Quá trình oxi hóa (sự oxi hóa) là quá trình nhường electron
- Quá trình khử (sự khử) là quá trình nhận electron
2. Cân bằng phản ứng oxi hóa – khử theo phương pháp thăng bằng electron
Dựa theo nguyên tắc: Trong một phản ứng, tổng số electron nhường bằng tổng số electron nhận.
Ví dụ: Cân bằng phản ứng Al + O 2 →Al 2 O 3
B1: Xác định sự thay đổi số oxi hóa trước và sau phản ứng của các nguyên tử
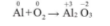
B2: Viết các quá trình oxi hóa và quá trình khử
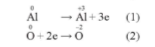
B3: Nhân thêm hệ số vào quá trình nhường, nhận sao cho tổng số electron nhường bằng tổng số electron nhận.
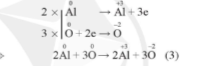
B4: Hoàn thành phương trình dạng phân tử
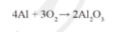
3. Ý nghĩa và một số phản ứng oxi hóa – khử quan trọng
* Phản ứng liên quan đến việc cung cấp năng lượng
- Phản ứng sinh ra năng lượng dưới dạng nhiệt khi đốt than:
- Quá trình hô hấp đã cung cấp oxygen để oxi hóa các chất sinh ra năng lượng:
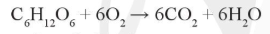
* Phản ứng liên quan đến việc lưu trữ năng lượng
- Phản ứng quang hợp
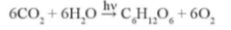
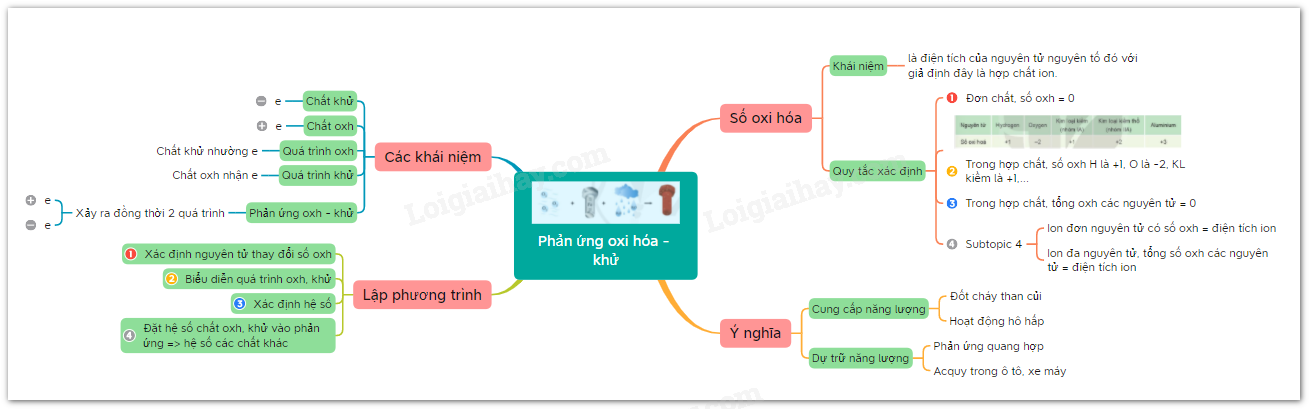
Sơ đồ tư duy